Inscription / Connexion Nouveau Sujet
Autoprotolyse de l'eau-pH-acide fort ,base forte
Bonsoir les amis 
J'aurais besoin d'aide pour cet exercice :
L'énoncé :
les questions sont indépendantes
1. À 10 cm3 d'une solution de chlorure d'hydrogène ,on ajoute 40 cm3 d'eau et on obtient alors une solution de pH = 2,7 .Quelle est la concentration de la solution de chlorure d'hydrogène initiale ?
2. Quel volume d'eau distillée doit-on ajouter à 40 cm3 d'une de chlorure d'hydrogène de concentration 2.10-2 mol/L pour obtenir une solution de pH =2,4 ?
3. On mélange 20 cm3 d'une solution chlorhydrique de pH =3,1 avec 10 cm3 de solution chlorhydrique de pH =2,3 .Déterminer le pH du mélange obtenu.
Merci de me guider
Bonsoir beugg.
L'acide chlorhydrique étant un acide fort, on peut considérer que dans un volume V d'une solution de concentration C de cet acide, on a [H3O+] = C et n(H3O+) = C V.
Pour résoudre les exercices que tu proposes, écris la conservation du nombre de mole d'ion H3O+ dans les mélanges étudiés c'est à dire 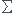 n(H3O+) avant =
n(H3O+) avant = 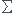 n(H3O+) après
n(H3O+) après
Je vais me déconnecter ce soir, essaie d'avancer un peu là dessus et mets tes résultats en ligne, je regarderai ce que tu auras fait demain (à moins que quelqu'un ne prenne le relais d'ici là).
À plus.
Merci Picard d'avoir répondu 
1/
Donc c'est comme on n'a pas besoin de prendre les données de l'énoncé.
Puisque [H3O+]= C
Or [H3O+]= 10-pH. ?
2/
Comme que le nombre de mole ne change pas donc ,on peut tirer volume d'eau distillée ?
Désolé ,je suis un peu étourdi !!
Désolé ,je suis un peu étourdi !!
Je vais te montrer comment procéder pour la première question, tu essaieras d'appliquer la même technique pour la suite...
1. À 10 cm3 d'une solution de chlorure d'hydrogène ,on ajoute 40 cm3 d'eau et on obtient alors une solution de pH = 2,7 .Quelle est la concentration de la solution de chlorure d'hydrogène initiale ?
La solution finale a un volume Vf = 10 + 40 = 50 mL = 50 10-3 L et son pH est 2.7.
On a donc, pour la solution finale, [H3O+]f = 10-pH = 10-2.7
 2.0 10-3 mol.L-1
2.0 10-3 mol.L-1
La quantité finale d'ion H3O+ dans cette solution est nf(H3O+) = [H3O+]f Vf
soit, numériquement : nf(H3O+) = 2.0 10-3
 50 10-3
50 10-3  1.0 10-4 mol
1.0 10-4 mol
Or :
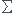 ni(H3O+) =
ni(H3O+) = 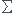 nf(H3O+)
nf(H3O+)
On sait que :
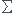 nf(H3O+) = 1.0 10-4 mol
nf(H3O+) = 1.0 10-4 mol
De plus :
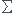 ni(H3O+) = n1(H3O+) + ne(H3O+)
ni(H3O+) = n1(H3O+) + ne(H3O+)
n1(H3O+) représente la quantité d'ion H3O+ apportée par les 10 mL de solution de chlorure d'hydrogène et on a : n1(H3O+) = C1 V1
ne(H3O+) représente la quantité d'ion H3O+ apportée par les 40 mL d'eau et on a : ne(H3O+) = [H3O+]e Ve
Comme pHe = 7.0, on a : [H3O+]e = 10-7 mol.L-1
Donc : ne(H3O+) = 10-7
 40 10-3 = 4.0 10-9 mol
40 10-3 = 4.0 10-9 mol
Soit, finalement : ni(H3O+) = C1 V1 + 4.0 10-9
En récapitulant, comme ni(H3O+) = nf(H3O+) on a : C1 V1 + 4.0 10-9 = 1.0 10-4
On tire alors : C1 V1 = 1.0 10-4 - 4.0 10-9
 1.0 10-4 mol (en fait, on néglige les H3O+ apportés par l'eau).
1.0 10-4 mol (en fait, on néglige les H3O+ apportés par l'eau).
et donc : C1 = 1.0 10-4 / V1 = 1.0 10-4 / 1.0 10-2 = 1.0 10-2 mol.L-1
Regarde ça et transpose le pour les autres questions.
Merci 
Q2,
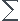 ni(H3O+)=
ni(H3O+)= 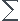 nf(H3O+) =>
nf(H3O+) =>
C1V1 +[H3O+]e*Ve = [H3O+]f*Vf
Or n1= nf =>
Vf= 0,2 L
Ainsi [H3O+]e= 10-7
Ensuite on a tiré Ve =0
Non ?
Je ne vois pas d'où tu sors la valeur de Vf = 0.2 L, mais c'est la bonne valeur !!!
Par contre, après, ça ne colle pas...
Ensuite on a tiré Ve =0
Je reprends l'énoncé...
2. Quel volume d'eau distillée doit-on ajouter à 40 cm3 d'une de chlorure d'hydrogène de concentration 2.10-2 mol/L pour obtenir une solution de pH =2,4 ?
Comme V1 = 40 mL, on n'aura pas Ve = 0.
A revoir.
Je ne vois pas d'où tu sors la valeur de Vf = 0.2 L, mais c'est la bonne valeur !!!.
[H3O+]f= 10-pH
n1= n(H3O+)f
C1V1= [H3O+]f*Vf
Vf= 0,2 L
Donc plutôt :
Ve= Vf- V1= 0,16 L ?
OK 
3/
Soient
[H3O+]1= 8.10-4 mol/ L
[H3O+]2= 5.10-3 mol/L
D'après la conservation, on a :
[H3O+]f= 2,2.10-3 mol/L
pHf= -log[H3O+]f
pHf= 2,6
C'est bon ?
Bien raisonné !
En mettant en mémoire, dans la calculatrice, les résultats intermédiaires avec toutes leurs décimales, j'obtiens pHf 2.7 (pH = 2.657), mais on ne va pas chipoter !
2.7 (pH = 2.657), mais on ne va pas chipoter !
Pardon !!
S'il s'agit d'une base forte,pour la conservation des matières, on fait la somme des ions OH- ?
Avant de répondre par oui ou par non, je préférerais avoir un exemple pour éviter de dire des sottises.
Ce n'est pas un exercice ça, il n'y a même pas de question.
De quoi s'agit-il, d'un mélange de plusieurs solutions de soude ?
Poste un énoncé complet s'il te plaît.



