Inscription / Connexion Nouveau Sujet
Alcane M=58 g/mol
Bonjour à tous !! ^^
Voila un nouvel exercice bien mystérieux...La consigne est simple, il y a pas de soucis :
" Je suis une alcane de masse molaire 58g/mol, identifiez moi."
A moins de les connaître toutes par par cur, je vois vraiment où aller avec simplement ça...
Si quelqu'un aurait une méthode, par ce que la je bloque bien...
Merci bien
Moi
Bonjour,
C'est tout bête : un alcane a une formule brute du type .
Quelle est l'expression de la masse molaire de l'alcane en fonction de n ? Sachant que tu connais la valeur numérique de sa masse molaire, tu peux en déduire la valeur de n et donc sa formule brute...
...
Ha wé...du coup je me sens c*n maintenant de pas y avoir pensé...^^
c'est fou ce qu'on fait avec rien...Je m'en souviendrai ^^
Merci beaucoup à toi...
Wé, j'ai trouvé C4H10
Ça me paraît correct^^
T'inquiète pas, je m'en rappellerai bien, il y a pas de soucis 
Pour le temps d réponse aussi, merci beaucoup

C'est ça 
Tu connais son petit nom ?
Et il possède des isomères. Je ne sais pas si d'autres questions étaient posées.
Le nom, non ( jeu de mot... )
)
Sérieusement, non, je ne le connais pas...
C'était la seule question, mais il y a un autre exercice que lequel je bloque bien, où il s'agit de reconnaître l'isomérie Z/E sur des alcanes que l'on nous propose comme 3-méthylbut-3-ène ( j'ai mis le nom que j'ai traduit de la formule semi-développée, donc... ), par exemple.
), par exemple.
Le truc, c'est que je ne comprends pas comment des différencier:
sur le cours c'est simple, il y a un truc simple avec 2 C, une double liaison entre, et soit 2 H d'un côté avec A et B de l'autre ( soit disant Z ) et l'autre c'est les mêmes 2 C, mais un H de chaque côté (et soit disant c'est E)
Sur celles du cour, c'est simple, mais sur les vraies molécules, il y a des H partout...
Pour différencier les isomères Z et E, il faut repérer les plus gros substituants sur chacun des carbones de la double liaison C=C.
(*) S'ils sont du même côté, alors il s'agit de l'isomère Z ;
(*) S'ils sont de part et d'autre de la double liaison C=C, alors il s'agit de l'isomère E.
Donc il faut regarder que les substituants rattachés aux carbones de la double liaison C=C ?
exemple:
CH3 - CH - C = CH - CH3
l l
CH3 CH3
On regarde que le CH3 en gras ?
Ton exemple ne va pas : les carbones sont tétravalents !
Prenons l'exemple du but-2-ène : .
(*) Soit les groupements 3$ -CH_3 sont du même côté de la double liaison carbone-carbone, et il s'agit alors du (Z)-but-2-ène ;
(*) Soit ils sont de part et d'autre de la double liaison, et il s'agit alors du (E)-but-2-ène.
Nan, mais sur votre exemple, il serait isomère E ?
Pour mon exemple:
CH3 - CH - CH = CH - CH3
l l
CH3 CH3
Ca ça existerai, si j'ai bien compris
Non, sur mon exemple il peut être les deux. Les formules semi-développées ne permettent pas de déterminer les isomères Z et E.
Il faut utiliser les formules développées ou topologiques.
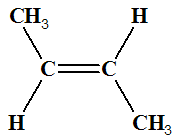
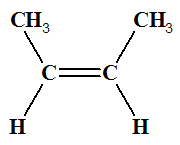
Quand on écrit la formule semi-développée, on ne précise pas de quel côté se trouve tel ou tel substituant : .
Alors qu'avec les formules développées (ou topologiques ça marche aussi), comme les deux images plus haut, on voit clairement de quel côté de trouve tel ou tel substituant. Si les deux plus gros sont du même côté de la double liaison, alors c'est le Z ; sinon c'est le E.
D'accord,...je pense que j'ai a peu près compris...Juste " les plus gros constituants" c'est bien que les CH3??
Pour être tout à fait correcte, il faudrait dire les substituants prioritaires. Et un carbone est prioritaire sur un un hydrogène (un atome de numéro atomique est prioritaire sur un atome de numéro atome plus faible) donc un groupement CH3 est prioritaire sur H.
Mais si tu avais un carbone de la double liaison relié d'un part à CH3 et d'autre part à C2H5, alors c'est C2H5 qui serait prioritaire.
Tu comprends ?
Donc les C prioritaire sur les H et si IL y aplusieurs C, c'est la molécule la plus riche en Carbone qui ets prioritaire ?
Pour mon exemple, ça revient à ça oui.
Mais dans le cas général, on regarde quels atomes sont reliés au carbone de la double liaison.
S'il y a un H et un C, on sait qu'un C est prioritaire sur un H donc c'est bon.
S'il y a deux C, il faut regarder "plus loin". Dans mon exemple, un de ces C est relié à un H alors que l'autre est relié à un autre C. Et comme un C est prioritaire sur un H, c'est donc le substituant avec les deux C qui est prioritaire.
Pour résumé : on regarde les premiers atomes reliés au C de la double liaison. Si on ne peut pas conclure, on s'intéresse aux atomes suivants, etc. Tu as suivi ?



