Inscription / Connexion Nouveau Sujet
Acide α aminés
Bonjour.
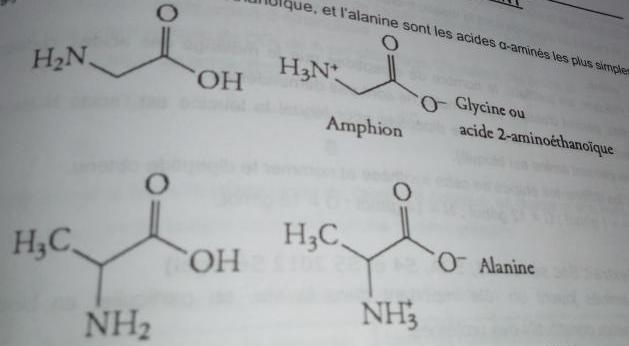
La glycine et l'alanine sont les acides α aminés les plus simples.
(images)
1. Identifier les groupes caractéristiques présents sur ces deux molécules.
2. En solution aqueuse il se forme presque exclusivement un ion bipolaire, appelé amphion (représenté dans le tableau précédent).
2.1. Définir un acide et une base selon Bronsted.
2.2. Quel est l'acide conjugué de cet amphion (on donne pKa1=9,9)?
Écrire alors l'équation de la réaction de cet amphion avec l'eau.
Quel est le rôle de l'eau ici ? Celui de l'amphion ?
2.3. Quelle est la base conjuguée de cet amphion (on donne pKa2=2,3)?
Écrire alors l'équation de la réaction de cet amphion avec l'eau.
Quel est ici le rôle de l'eau et celui de l'amphion ?.
2.4 . Comment peut on qualifier cet amphion ?
3.les valeurs des pKa des couples acido -basiques sont pKa1=2,3 et pKa2=9,9.
3.1.Sur un axe,indiquer les domaines de prédominance de chaque couple de l'alanine.
3.2. On acidifie la solution aqueuse de l'alanine, on obtient un ph de 2. Quelle est l'espèce majoritaire ? Que se passe-t-il si la solution a un ph=6, un ph=11 ?
Mes réponses
1.lew groupes caractéristiques présents sur ces deux molécules sont le fonctionnel carboxyle -cooh et le groupe fonctionnel amine -NH2.
2.
2.1.DEFInition c'est des questions de cours.
2.2 là je suis bloqué car la figure montre deux amphion différents.
Que faire?
Bonjour
2.2 là je suis bloqué car la figure montre deux amphion différents.
Tu as raison : la figure fournit les formules développées pour la glycine et pour l'alanine alors que toutes les questions à partir de la n° 2 concernent un seul acide aminé. Cet énoncé n'est pas très clair.
Cependant, si on lit la totalité de l'énoncé, question 3.1 en particulier, on "devine" que cet exercice concerne essentiellement l'alanine, la glycine intervenant seulement à la première question.
Sous toutes réserves bien sûr...