Inscription / Connexion Nouveau Sujet
temperature d'ebulition
Salut les amies je sais que plus la chaine carbonee est grande et plus la temerature d'eblution augmente
est ce que on peut me corriger
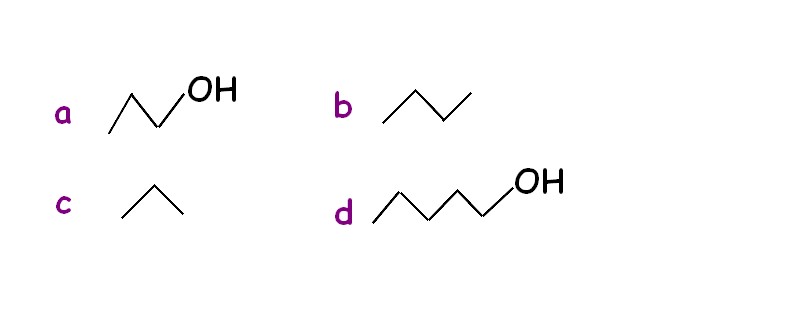
Ranger dans par ordre croissant ces composes suivant leur température ébullition
ordre : c a B d
Bonjour,
La température d'ébulition, dépend de deux facteurs qui sont :
 La masse moléculaire, plus celle ci est élevée, plus la température d'ébullition sera importante.
La masse moléculaire, plus celle ci est élevée, plus la température d'ébullition sera importante.
 Les liaisons inter-moléculaires, qui peuvent s'opérer, plus il y a de liaisons inter-moléculaires, plus la température d'ébullition sera importante.
Les liaisons inter-moléculaires, qui peuvent s'opérer, plus il y a de liaisons inter-moléculaires, plus la température d'ébullition sera importante.
Donc ? 
Ah oui, j'oublié... vous avez effectivement raison, sur le fait que plus la chaîne carbonée est grande, plus la température d'ébullition le sera également.
Non 
C'est C , B , A et D.
Le deuxième principe :
Les liaisons inter-moléculaires, qui peuvent s'opérer, plus il y a de liaisons inter-moléculaires, plus la température d'ébullition sera importante.
Ce principe l'emporte sur la taille de la chaîne carbonée, je m'explique ..
Vous commencez dans un premier temps, par observé, dans quelles molécules peut s'opérer des liaisons inter-moléculaires, ici les liaisons H dût au groupe hydroxyle -OH  voir molécule a) et d).
voir molécule a) et d).
Par conséquent, c'est elles qui posséderont un point d'ébullition élevé.
Il vous reste par conséquent deux autres molécules, des alcanes, où aucunes liaisons inter-moléculaires n'est possible.
Ainsi, cela ce joue sur la chaîne carbonée, la molécule c) le propane possède une chaîne carbonée plus petite que la molécule b) le butane.
Ainsi vous avez déja C < B < A < D
J'espère que mes explications étaient claires ? 
Bonne journée 
je n'ai pas compris liaisons inter moleculaires !
c'est les OH ? plus il ya d'OH et plus leur temperature augmente ?
Oui, ici il est question de liaisons hydrogène.
Savez-vous ce qu'est qu'une liaison hydrogène ?
Le fait qu'une liaison inter moléculaire se manifeste au sein d'une molécule, la température d'ébullition augmente.
Donc vous avez la molécule a) et d).
Or parmi ces deux molécules, la molécule a), le propan-1-ol, possède une chaîne carbonée plus courte que celle de la molécule d), le pentan-1-ol.
C'est pour cela que on a : a < d
Vous avez compris ?
oui bah une liaison d'hydorgene tout simmplement 
liaison inter moleculaire en 1 phrase c'est quoi ? les OH par exemple ?
sinon oui j'ai compris !!!!!!!!!
Oui c'est tout à fait ça, vous avez également les liaisons de van der waals et j'en passe ..
Ce sont tout simplement des interactions entre molécules.
okeii mais en faite les liason hygrogene elle doivent etre successive je veux dire par laa à la suite ou il peut avoir dans une molecule un atome qui n'a pas de liasons d'hydrogene
je ne comprend pas du tout la b ...... :/ j'ai revu ce qu'est une liason hydrogene mais comment peut ton savoir qu'il yen a ? !!
Une liaison hydrogène n'est pas... une liaison avec un H, n'est ce pas ?
Une liaison hydrogène s'établie entre un Hydrogène et un autre atome ayant une différence d'électronégativité , par exemple l'oxygène .. comme dans les molécules a) et d).
Dans votre molécule b), vous avec des H, mais on ne peut pas parler de liaison hydrogène avec le carbone car la différence d'électronégativité entre les deux atomes est bien trop faible .
Pour le carbone :2,5 et l'hydrogène : 2,1 , ainsi 0,4 ne suffit pas contrairement à l'oxygène : 3,5.
Vous avez compris ?
Ahhhhhhhhhhh okeiiiiiii d'accoooord !!!!!
LA LIAISON HYDROGENE(liason intermoleculaire) ELLE EST ENTRE OH on est d'accord ?


