Inscription / Connexion Nouveau Sujet
Spectre de raie d'emission
Bonjour, j'ai un problème pour la réalisation d'un exercice de physique:
Il faut donner l'expression littérale de la fréquence d'un photon émis lorsque l'atome retourne à l'état fondamental, en étant initialement dans son premier état excité, puis la longueur d'onde de ce photon avant d'appliquer.(Nous travaillons sur une lampe à vapeur d'hydrogène).
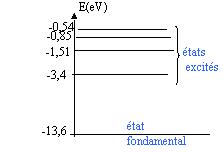
Un diagramme nous est fourni en complément montrant que:
E0=-13,6 E1=-3,40 E2=-1,51 E3=-0,85 E4=-0,54 E5=-0,37 Einfini=0
Nous savons que E=h*v donc v=E/h puis lambda=c/v
Donc v=3,40/constante de Planck
v=5,13*1033
Et je finis par trouver lambda=5,83*10-26mètre...
Ce qui n'est pas du tout cohérent. Mais je n'arrive pas à trouver ma ou mes erreurs.
Merci beaucoup de vôtre aide
Salut  !
!
Effectivement c'est une longueur d'onde aberrante et c'est très bien de s'en rendre compte
E = (hc)/ ok mais d'où sort v = 3,40/h? Du premier niveau d'excitation exprimé en eV?
ok mais d'où sort v = 3,40/h? Du premier niveau d'excitation exprimé en eV?
Tu as bien pris h=6,62.10-34 J.s?
Les échanges d'énergies entre la lumière et la matière ne se font pas de manière continue mais par quantité élémentaire. Une transition atomique est le passage d'un état d'énergie à un autre. La fréquence d'un photon émis ou absorbé est reliée aux énergies En et Ep par la relation de Bohr :
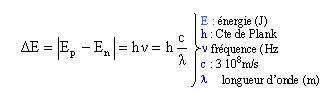
Chaque raie d'un spectre est associée à l'émission ou l'absorption d'un photon lors d'une transition atomique.
Bonsoir,
Donc l'expression littérale de la fréquence du photon émis lorsque l'atome retourne à l'état fondamental, en étant initialement dans le premier état excité est:
E=h(c/v) = 6,63*10-34*(3*108/6,56*10-7) = 3,03*10-19
Ceci est donc la fréquence exprimée en Hertz. Est-ce bien cela?
Nous pouvons en déduire que lambda=c/v
Ce que je ne comprend pas est le fait qu'ensuite, j'ai un tableau à remplir comme ceci:
Etat initial de l'électron: Etat excité 1 ... Etat excité 4
Longueur d'onde du photon émis lors du retour à létat fondamental //
Je ne vois pas comment le remplir, je pense qu'il y a quelque chose que je n'ai pas compris, mais je ne sais pas quoi.
Merci beaucoup
Je crois que tu n'as pas compris mon message subliminal (désolé j'ai encore le cerveau embrumé) : tu calcules ta transition  E en eV (tu fais la différence des deux), que tu converties en J
E en eV (tu fais la différence des deux), que tu converties en J
Puis  = hc /
= hc /  E
E
J'ai le même problème. Je crois (svp, dites moi si c est correcte ou pas), qu'il faut calculer le lambda de passage de l etat 2 (premier état excité) au fondamental, de l etat 3 (2eme état excité) au fondamental, etc.
J'obtiens:
Lambda = 1,22 x 10-7 pour le retour du premier état éxcité au fondamental ( E = 13,6-3,39)
E = 13,6-3,39)
Lambda = 1,03 x 10-7 pour le retour du 2ème état éxcité au fondamental ( E = 13,6-1,51)
E = 13,6-1,51)
Lambda = 9,75 x 10-8 pour le retour du 2ème état éxcité au fondamental ( E = 13,6-0,85)
E = 13,6-0,85)
Lambda = 9,52 x 10-8 pour le retour du 2ème état éxcité au fondamental ( E = 13,6-0,54)
E = 13,6-0,54)
On peut pas le voir sur le spectrum, en fait!
Johnny
mince répondue trop tôt...
cbv ---> un exemple :
L'énergie d'ionisation de l'atome d'hydrogène est l'énergie qu'il faut fournir pour arracher l'électron soit 13,6 eV.
transition n=5 à n=3 : l'énergie de l'atome diminue, un photon est émis
 E = 1,511-0,544 = 0,967 eV ou 0,967*1,6.10-19 = 1,547.10-19 J
E = 1,511-0,544 = 0,967 eV ou 0,967*1,6.10-19 = 1,547.10-19 J
longueur d'onde du photon émis :  = hc/
= hc/ E
E
 = 6,62.10-34*3.108/1,547.10-19 = 1,28 10-6 m
= 6,62.10-34*3.108/1,547.10-19 = 1,28 10-6 m
Tu peux même en conclure que tu es dans le domaine des UV
Pour les applications numériques je vous fait confiance, du moment que les ordres de grandeurs sont corrects
jtorresm : je ne trouve pas du tout les mêmes valeurs de lambda que toi, comment ça se fait?
J'ai trouvé 1,95.10-26 m pour le premier par exemple...



