Inscription / Connexion Nouveau Sujet
Schéma pile cuivre plomb
Bonjour à tous, toutes,
Je suis confronté à un problème sur lequel je travail depuis plus de deux heures sans trouver de réponses à ma question. Voici l'énoncé de mon exercice :
Dans un bêcher on met en présence une solution bleue de sulfate de cuivre avec une solution incolore de sulfate de plomb. On plonge une lame de plomb et un fil de cuivre dans le milieu obtenu. Après quelques minutes, on observe la décoloration de la solution et un dépôt rouge sur la la lame de plomb.
A l'aide de cet énoncé je dois répondre aux questions suivantes :
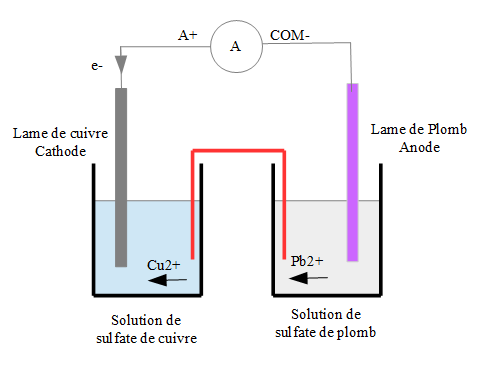
1- Schématiser la pile que l'on peut réaliser à l'aide de ces couples oxydant/réducteur.
2- Faire figurer sur le schéma un ampèremètre de telle façon que l'intensité du courant qui le traverse soit lue positivement.
3- Faire apparaître sur le schéma le mouvement de tous les porteurs de charges.
Voilà mon schéma, en sachant que l'équation de l'oxydoréduction est Pb(s) + Cu2+(aq) --> Pb2+(aq) + Cu(s) :
Je ne sais pas s'il est correct. Malgré tout, si ce schéma est correct, je ne comprends pas pourquoi un dépôt rouge se forme sur la lame de plomb alors que les ions cuivre captent des électrons auprès de la lame de cuivre (c'est à dire que du cuivre se forme sur cette même lame de cuivre...).
Pouvez-vous m'aider ?
Merci d'avance
Bonjour.
Je vous confirme que ce que vous avez fait est correct. Votre schéma correspond bien à une pile cuivre-plomb.
Le dispositif décrit en préambule à l'exercice N'EST pas une pile : les électrons sont transférés directement des atomes de plomb Pb (qui les cèdent) aux ions Cu2+ (qui les reçoivent) ; il y a bien dépôt de cuivre métal Cu sur la lame de plomb (en contact direct avec la solution)
Dans la pile, les électrons ne sont pas transférés directement des atomes de plomb aux ions cuivre, les électrons "voyagent" à travers le circuit électrique depuis la lame de plomb (qui va se dissoudre petit à petit) jusqu'à la lame de cuivre, où ils seront captés par les ions cuivre qui seront alors réduits en atomes de cuivre métal ; la masse de la lame de cuivre va progressivement augmenter, alors que la solution va d'appauvrir en ions cuivre.
OK ?
Merci de votre réponse claire et simple, seulement, une question subsiste :
Le schéma que j'ai fait est bien une pile, mais, le dispositif décrit dans l'énoncé n'en est pas une, ce que je n'avais pas bien compris (et oui, on perd des informations à vouloir lire trop vite...). Est-ce que cela signifie que l'énoncé nous décrit la situation suivante (voir schéma) ?
Je voulais vous demander si mes explications sont correctes :
(Dans le cas où le schéma précédent est correct) Il paraît logique que la lame de plomb soit couverte d'un dépôt de cuivre car cette lame est en contact direct avec les ions cu2+, et cèdent des électrons (ainsi que des ions Pb2+).
Mais dans la pile, nous n'observons pas de dépôt de cuivre sur le plomb car les ions cu2+ se situent près de la lame de cuivre, et les électrons cédés par la lame de plomb, circulent jusqu'à la lame de cuivre. Nous observons donc (comme vous l'avez dit), une augmentation de la masse de Cu et une diminution de la masse de Pb.
Enfin, nous en venons à ma question, que fait la lame de cuivre présente dans le schéma que je viens de réaliser ? Est-elle seulement ''spectatrice'' ?
Encore merci pour votre réponse
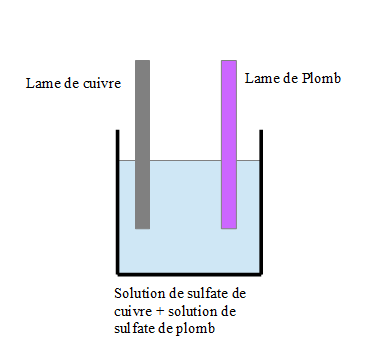
Oui, c'est bien ce dispositif (celui que vous avez représenté dans votre post de 11h06) qui est décrit dans l'énoncé. Comme vous le dites, la lame de cuivre, ainsi d'ailleurs que les ions Pb2+, sont spectateurs ; on observerait les mêmes résultats (réduction de Cu2+ et oxydation de Pb) en plongeant simplement une lame de plomb dans une solution de sulfate de cuivre.
L'intérêt de la pile est de "forcer" les électrons à traverser le circuit électrique (qui se réduit ici à l'ampèremètre) pour passer des atomes de plomb aux ions Cu2+.
OK ?
Merci beaucoup, vos explications m'ont été d'une grande aide.
Si je puis me permettre j'ai une dernière question qui n'est pas mentionnée que je viens de me poser. Si nous inversions dans la pile la position des deux solutions (solutions de sulfate de cuivre et solution de sulfate de plomb) que se passerait-il ? Cela change-t-il quelque chose (par exemple, pourrions nous trouver un dépôt de cuivre sur la lame de plomb, ou les ions cu2+, iraient-ils vers la lame de cuivre ?)
Merci de me consacrer de votre temps !
Si nous inversions dans la pile la position des deux solutions (solutions de sulfate de cuivre et solution de sulfate de plomb) que se passerait-il ?
Dans ces conditions, aucun courant ne traverse le circuit, le dispositif ressemble à une pile, mais ce n'en est pas une...
Bonjour.
Je ne comprends pas pourquoi le cuivre subit une réduction et non une oxydation ? Pouvez-vous m'aider ? Merci.
Pour moi le dépôt rouge c'est dû aux ions Cu2+. Il perd donc des ions du coup c'est une oxydation...
Le dépôt rouge est un dépôt de cuivre métallique Cu(s)
Ce cuivre métallique provient de la transformation des ions Cu2+ en atomes de cuivre.
Cette transformation peut être modélisée par la 1/2 équation : Cu2+ + 2e-  Cu(s) qui se produit à la cathode.
Cu(s) qui se produit à la cathode.
Cette transformation est un gain d'électrons : C'est une réduction
Désolé mais j'arrive pas à comprendre pourquoi le dépôt rouge c'est du cuivre. Et que c'est un gain d'électrons et non une perte...
Il n'y a pas à essayer de comprendre pourquoi le dépôt rouge est un dépôt de cuivre.
Quand on fait l'expérience on constate la formation d'un dépôt rouge.
Si on recueille ce dépôt et qu'on l'analyse on constate que ce dépôt rouge est constitué par du cuivre.
D'autre part il est notoire que le cuivre est un métal de couleur rouge.
Même si on ne comprend pas pourquoi, aucun doute ne subsiste et il faut bien se rendre à l'évidence : Ce dépôt rouge est bien du cuivre.
Ce cuivre provient du fait que des ions cuivre ont gagné des électrons pour devenir des atomes de cuivre.
Il s'agit d'un gain d'électrons.


