Inscription / Connexion Nouveau Sujet
Réaction de combustion, tableau d'avancement
Bonjour, j'ai besoin d'aide car je ne comprend pas comment procéder pour réussir cet exercice :
Merci d'avance pour votre aide
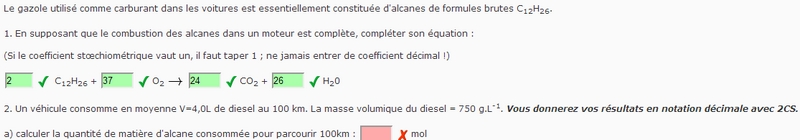

Bonjour
le véhicule consomme 4L au 100km soit 0,04L par km
l'alcane est C12H26, sa masse molaire est MC12H26 = 12*12+26 = 170 g.mol-1
la masse volumique de l'alcane est 750g/L, la masse d'alcane nécessaire pour rouler 1 km est donc de:
0,04*750 = 30g
le nombre de mole de C12H26 est donc de 30/170 = 0.18 mol
Test mais du coup je sais plus si faut multiplier après ou pas. Je laisserais comme ça.
Merci beaucoup, la réponse était donc de 18 mol.
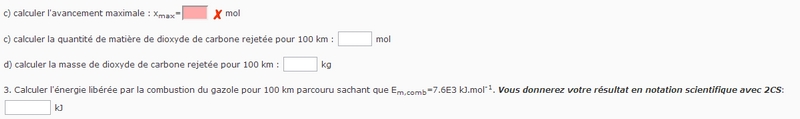
Donc Xmax=9 mol
Par contre je ne sais pas comment calculer la quantité de dioxygène produit



