Inscription / Connexion Nouveau Sujet
Réaction doxydo-réduction
Bonjour, pouvez vous m'aidez s'il vous plaît j'ai du mal à faire cet exercice, merci d'avance.
L'équation bilan de la réaction est :
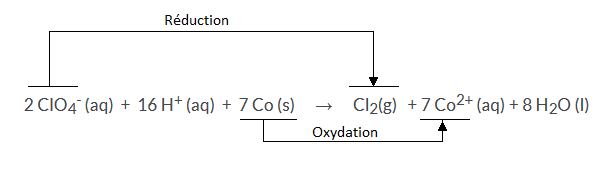
2 ClO4- (aq) + 16 H+ (aq) + 7 Co (s) → Cl2(g) + 7 Co2+ (aq) + 8 H2O (l)
1. Par 2 flèches annotées : l'oxydation et la réduction.
2. Le nom de l'oxydant, le nom du réducteur de la réaction.
3. Le nom du réducteur conjugué de l'oxydant. Puis celui de l'oxydant conjugué du réducteur.
Mes recherches :
1. Je pense que la flèche oxydation va de 7 Co à 7 Co2+ , car selon moi 7 Co est l'oxydant et 7 Co+2 est le réducteur. Est-ce correct ?
Pour la flèche réduction, j'ai un doute, car 2Cl04- perd aussi des électrons pour s'être transformé en Cl2 , du coup ça serrait aussi une oxydation. Je pense que je me trompe.
Bonjour,
Voir mon schéma.
Justifications possibles soit en écrivant les équations des demies réactions soit par la méthode des nombres d'oxydation.
Bonjour, merci pour votre réponse !
Du coup si je comprends bien 7 Co est l'oxydant et 7 Co+2 est le réducteur.
Et pour l'autre, 2Cl04- est le réducteur et Cl2 est l'oxydant. C'est bien ça ?
Pourriez vous m'expliquez la question 3 s'il vous plaît car j'ai du mal à la comprendre.
Il n'y a pas à tenir compte des coefficients stchiométriques ( 7 et 2 ) pour désigner l'oxydant et le réducteur .
Si tu relis ton cours tu devrais y trouver que :
L'oxydant subit une réduction, c'est-à-dire qu'il gagne des électrons et se transforme en son réducteur conjugué.
Le réducteur subit une oxydation en perdant des électrons et se transforme en son oxydant conjugué.
On peut résumer cela par le schéma général suivant :
Oxydant 1 + Réducteur 2 --> Réducteur 1 + Oxydant 2
le réducteur 1 est le réducteur conjugué de l'oxydant 1 tandis que l'oxydant 2 est l'oxydant conjugué du réducteur 2
Tu as là tout ce qu'il te faut pour proposer des réponses argumentées aux questions 2 et 3

 s'il vous plaît
s'il vous plaît
