Inscription / Connexion Nouveau Sujet
Radioactivité et réactions nucléaires
Bonsoir,
Je suis en première S et j'ai un exercice à faire que je ne comprends pas très bien.
L'énoncé est le suivant :
L'iode intervient dans le métabolisme de la glande thyroïde. L'iode 127 (127 I) est stable, alors que l'iode 131
(53 )
est émetteur beta+ et l'iode 124 est émetteur beta -.
1. Ecrire les équations des désintégrations de l'iode 131 et de l'iode 124.
2)a. Calculer le défaut de masse de ces trois noyaux isotopes de l'élément iode en unité de masse atomique puis en kilogrammes.
b. Calculer les énergies de liaison de ces 3 isotopes en joule puis en mégaélectronvolt.
c. Quelles sont les énergies qu'il faut fournir à un noyau au repos pour le dissocier en nucléons isolés,au repos ?
3)a. Calculer les énergies de liaisons par nucléon.
b. Classer les isotopes selon leur stabilité. Le résultat est-il en accord avec les propriétés radioactives de certains isotopes ? Justifier.
Données: Masse des nucléons : m neutron= 1,00866 u ; m proton= 1.00728 u
Masse des noyaux : m iode 124= 123,877 10 u ; m iode 127= 126.875 53 ; m iode 131= 130, 876 97 u
avec 1 u= 1,66055.10 puissance-27 kg ; 1eV= 1,6022.10 puissance-19 J ; c= 2.9979.10 puissance8 m.s puissance-1
Bonjour,
Comment peut-on savoir ce que tu ne comprends pas puisque tu ne proposes aucun résultat ?
Je ne pense pas que tu souhaites que quelqu'un fasse ton travail à ta place...
___________
Peux-tu vérifier soigneusement l'énoncé que tu as posté ?
Je ne crois pas que l'iode 131 soit émetteur  +
+
ni que l'iode 124 soit émetteur  -
-

Dans l'énoncé, j'ai bien l'iode 131 qui est émetteur beta+ et l'iode 124 qui est émetteur beta-
Oui je m'excuse, je suis désolé je n'ai pas précisé ce que je n'ai pas compris.
1) Désintégration de l'iode 131 : 131 I ==> 127 I + 4 ... Mais ne n'arrive pas à trouver ce que ça peut être, on
53 53
doit ajouter à un électron non ?
2)a. Défaut de masse de l'iode 127 I = Dm= [Z.mp+(A-Z).mn]- mnoyau
53
= [53x1,67.10puissance-27 + (127-53)*1.67.10puissance-27]- 2,11.10puissance-25
= 1,09.10puissance-27 kg => je trouve ça, l'nuté de masse atomique, est-ce ''u'' ?
b. El= Dm x c²
= 1,09x10puissance-27 * 2,9979x10puissance8²
= 9,796270807x10puissance-11 = 9,80x10puissance-11
1) L'iode 124 I ==> 127 I + ? +> Je ne vois pas ce qu'on pourrais mettre, ici aussi ça doit être un électron non ?
53 53
Il y a comme un malaise
Je suppose que l'exercice a été recopié d'un site où il y a de multiples erreurs comme par exemple ici : ![]()
On y dit bien que l'iode 131 est émetteur beta+ et l'iode 124 est émetteur beta- ...
On trouve cette info sur une multitude de site... Oui, mais c'est faux.
Quand une connerie est écrite sur internet, elle se retrouve recopiée en de multiples endroits.
***
L'iode 131 est emetteur Beta- et l'iode 124 est émetteur Beta+
Voila un site (parmi aussi plein d'autres) qui donne l'info correcte : ![]()
On y voit, par exemple ce tableau :
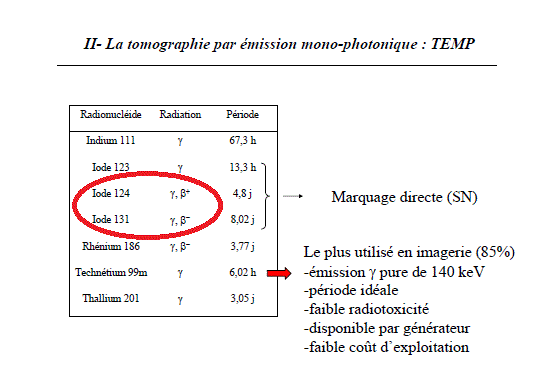
************************
Le problème est maintenant celui-ci :
Pour la question 1, as-tu besoin de la bonne solution ou bien de celle probalement attendue, mais qui est fausse ? 
*****
Sauf distraction. 
Ah oui, vous avez raison ! Je voudrais bien avoir la bonne solution, est-ce celle la pour "celle probablement attendue mais qui est fausse" ?
131 I ==> 131 I + 0 e
53 54 -1
124 I ==>131 Te + 0 e
53 52 1
Comment calculer une désintégration ?
Si c pour un émetteur beta+, nous devons ajouter un positon avec A=1 et Z=0 aux produits
pour un émetteur beta-, nous devons ajouter un électron avec A=0 et Z=-1 aux produits
pour un émetteur alpha, nous devons trouver l'élément qui s'associerais avec le produit pour donner le(s) réactif(s) ?
Bonjour et merci J-P 
Samia >>
L'atome dont le noyau a 53 protons est un atome d'iode (Z = 53 est le numéro atomique de cet atome)
L'atome dont le noyau a 54 protons n'est plus un atome d'iode, mais un atome de xénon.
Tu as correctement noté que l'atome dont le noyau a 52 protons est un atome de tellure.
Radioactivité  -
-
(et un antineutrino
que tu es certainement autorisé(e) à ignorer)
Radioactivité  +
+
(et un neutrino
que tu es certainement autorisé(e) à ignorer)
On passe à la question 2...

Je vois que tu as proposé des réponses pour la question 2
Ce n'est pas cela.
L'unité de masse atomique a en effet pour symbole u
Dm= [Z.mp+(A-Z).mn]- mnoyau
Ceci est correct
Il faut faire tous les calculs dans cette même unité u (on te donne, exprimées dans cette unité, les masses du proton, du neutron et de chaque noyau) et conserver tous les chiffres significatifs donnés par l'énoncé pour avoir des résultats corrects (ne surtout pas arrondir les valeurs intermédiaires ! ).



