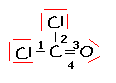Inscription / Connexion Nouveau Sujet
molécules et liaison covalente
bonjour
le phosgéne formule chimique CL2 CO
n atomique de Carbone 6/Oxygene 8 et Clore 17
ils possédént 24 electrons externes donc 12 doublets
je ne sais pas repondre aux questions suivantes
combien d'électrons manquent ils pour devenir une structure stable ?combien l faut il établir pour obtenir cette structures?
preciser les doublets liants et non liants?comment puis je faire? sur ma representation de lewis,je ne trouve pas les 12 doublets
je demande de l'aide car je viens d'y passer 2 heures et je n'ai toujours tpas trouver
merci de votre aide ,de tout et bon coeur


Bonsoir Elober,
Je ne comprends pas trop les questions qui te sont posées, mais la représentation de Lewis de Cl2CO est celle que je te mets en pièce jointe. En rouge, les doublets non liants et en noir, les doublets liants.
bonjour
merci à orsolya
pouvez vous me dire le calcul des doublets liants et non liants sur l'exercice du CL2CO que j'ai posté le
24/ 1/07
l'exercice est pour demain
merci d'avancepour votre aide

Tu as deux atomes de 17Cl. Les électrons externes, ceux qui se situent sur la couche de valence sont au nombre de 7*2 soit 14. (Il suffit de compter combien tu peux en caser dans les couches K(2), L(8), etc.
Ensuite tu as un atome de 6C, avec 4 électrons externes.
Et enfin tu as un atome de 8O, avec 6 électrons externes.
Donc au total tu as bien 14+6+4 = 24 électrons externes.
On divise par 2 pour avoir le nombre de doublets : 12
Tu dessines ta molécule en sachant qu'un C compte 4 liaisons, qu'un Cl en compte 1 et qu'un O en compte 2.
Ces liaisons seront en fait les doublets liants.
Ici, l'atome central est le C, donc tu places quatre doublets liants tout autour, il te restera 12-4 = 8 doublets non liants à diposer autour des autres éléments.
je te remercie orsolya
je vais m'entrainer en suivant tes conseils
elober
De rien.
Je t'encourage à lire ce que j'ai déjà expliqué sur les doublets liants et non liants : ![]() Chimie:Comment déterminer le nombres de doublets non-liants (clique sur la petite maison).
Chimie:Comment déterminer le nombres de doublets non-liants (clique sur la petite maison).
D'après ce que j'ai expliqué plus haut, l'atome de carbone fait 4 liaisons et l'atome d'oxygène en fait deux. Or, les deux constituants (en l'occurence, les Cl) ne peuvent former que 2 liaisons avec C. Donc l'oxygène n'a pas d'autre choix que de former une double liaison pour permettre la stabilité du carbone (donc pour lui permettre d'avoir les 4 liaisons qu'il demande). L'oxygène fait deux liaisons, mais qu'il fasse deux liaisons simples ou un double revient au même.