Inscription / Connexion Nouveau Sujet
Justifier charges portées par latome dazote dans chaque ions
Bonjour,
Voici un exercice sur lequel je suis bloqué depuis une bonne semaine j'ai réussi le 1) mais le 2) reste incompréhensible pour moi quelqu'un pourrait éventuellement m'aider svp ?
** image supprimée **
Le règlement de ce forum, que tu sembles ignorer, ne permet pas de publier un énoncé sous forme d'images.
De plus, ce même règlement demande expressément de montrer le travail déjà fait.
Tu aurais pu par exemple donner les solutions que tu as trouvées pour la question 1
Comme ces solutions se présentent sous forme d'images, tu peux cette fois utiliser ce mode de publication sans enfreindre le règlement.
Dans la mesure où tu fais le nécessaire pour respecter le règlement, je me ferai un plaisir de t'apporter l'aide que tu demandes.
Attention, ne crée pas un nouveau topic : Les double - posts sont également interdits.
D'ailleurs, le plus simple serait de (re)lire ce règlement et .... de le respecter.
Merci de m'avoir expliqué, à vrai dire je viens tout juste d'arriver sur ce site désolé, l'exercice qui pose problème est le suivant :
L'hydrazine est utilisée comme carburant de fusée. Sa molécule est formée uniquement de quatre atomes d'hydrogène et de deux atomes d'azote. La molécule de diazène à deux atomes d'hydrogène en moins.
1) établir les schémas de Lewis des deux molécules.
2) les ions diazedine a) et diazenylium b) ont pour schéma de Lewis : voir photo jointe.
J'ai réussi le 1) d'après moi (voir photo jointe) mais le 2) me pose problème puisque je ne vois pas quoi faire cela fait pourtant une bonne semaine que je suis sur cet exercice.
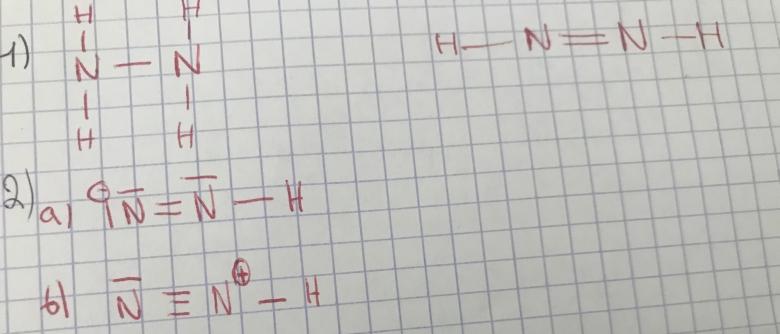
Pardon j'ai oublié la suite de l'énoncé du petit 2 : justifier les charges portées par l'atome d'azote dans chaque ion.
Merci d'avance
Il semble bien que tu n'aies rien compris à mes explications.
Il est interdit de publier un énoncé sous forme de photo.
Tu as donc recopié cet énoncé : ça c'est parfait !
Mais en même temps tu joins une photo qui contient cet énoncé !
Un modérateur a supprimé ta première photo (post du 23-10-19 à 16:00)
Il va plus que probablement recommencer sur ta deuxième photo !
C'est à toi de cadrer les images de manière que le texte n'apparaisse pas !
Et ce n'est pas tout :
Dans mon post du 23-10-19 à 16:44 je te disais que le règlement demande expressément de montrer le travail déjà fait et que tu aurais pu par exemple donner les solutions que tu as trouvées pour la question 1
Je ne trouve aucune trace de ce travail.
C'est assez désagréable de perdre son temps avec des demandeurs d'aide qui ne lisent pas le règlement ou bien qui le lisent et n'en tiennent aucun compte !
Euux enfaite mon travail il est sur la photo hein et je l'ai meme dit dans mon texte qu'il est sur la photo, regarde le 1) de la photo c'est mon travail c'est le 2) qui est l'image de l'énoncé
Nan plus sérieusement j'ai fais quelque chose mal là ? Si c'est le cas dis le moi et j'en suis vraiment désolé hein
Je viens de comprendre et je retire tout ce que j'ai dit et je te présente mes excuses !
L'explication est la suivante :
Le cache de mon ordinateur avait gardé en mémoire ta première photo (celle qui a été supprimée ).
C'est cette photo (la fusée + l'énoncé) qui s'est affichée avec ton dernier message à la place de ton travail, d'où ma réaction.
Ayant compris, j'ai vidé le cache de mon ordinateur qui aussitôt a affiché la bonne photo contenant ton travail.
Ton travail concernant l'hydrazine et le diazène est presque exact :
Hydrazine N2H4
Chaque atome d'azote possède 5 électrons périphériques et chaque atome d'hydrogène 1 seul, cela fait au total (2*5) + (1*4) = 14 électrons à répartir sous forme de 14/2 = 7 doublets électroniques.
Or ta molécule d'hydrazine ne possède que 5 doublets. Il lui en faut 7
Tu dois donc rajouter les doublets non liants portés par les atomes d'azote.
Chaque atome d'azote sera alors entouré de 4 doublets ( 2liants et 2 non liants) soit 8 électrons conformément à la règle de l'octet.
L'explication ci-dessus peut être répétée pour la molécule de diazène afin là aussi de corriger ce que tu as fait.
Et puis toujours en appliquant ce raisonnement, il n'est pas impossible que tu puisses trouver par toi même la réponse à la question 2.
Je te laisse y réfléchir.
Ah cool, tout s'explique je pensait avoir encore enfreint le règlement entouca merci pour ta correction !
Pour ce qui est du 2) après avoir fait le schéma de Lewis je m'aperçois qu'il a des électrons soit supplémentaire qd c'est négatif soit qu'il en manque lorsque c'est positif cependant je n'ai pas d'explication à proprement parler. Éventuellement le milieu ? Ou cette piste est à écarter ?
L'ion a) comporte 2 atomes d'azote et 1 atome d'hydrogène soit (2*5) + 1 = 11 électrons périphériques.
Sur la figure donnée par l'énoncé on compte 6 doublets donc 12 électrons, soit un de plus que ceux apportés par les atomes.
L'ensemble de la structure (et pas forcément l'atome d'azote) s'est "débrouillée" pour "piquer" dans son environnement 1 électron supplémentaire et c'est ce qui explique la charge négative.
Tu devrais maintenant pouvoir résoudre tout seul le cas de l'autre ion.
Je t'engage vivement à rédiger une solution et ne pas te contenter d'évoquer vaguement "un électron en plus" ou un "électron en moins"


