Inscription / Connexion Nouveau Sujet
Ion chlorure dans l'eau de mer
Bonjour !! J'aurai besoin de votre aide SVP =D !! ( Ne vous inquiétez pas,ça parait long mais en fait c'est surtout l'énoncé qui prend de la place :p)
L'Artémia est un petit crustacé qui a besoin de vivre dans un milieu marin dont la concentration massique (ou teneur) moyenne des ions chlorure Cl- est supérieur à 30 g.L-1.
Avant d'implanter un élevage d'artémia dans des marais salants, on se propose de déterminer la concentration des ions chlorure d'un prélèvement d'eau d'un marais de la zone choisie (sud de la France). Cette eau contient exclusivement des ions sodiums et des ions chlorure.
A- Principe de titrage
On veut titrer un volume V1 d'une solution S1 d'ions chlorure par une solution S2 de nitrate d'argent, de concentration apporté en soluté C2. Les ions chlorure réagissent par précipitation avec les ions Ag+. Le chlorure d'argent formé est un solide blanc. La transformation est modélisée par l'équation : Ag+(aq) + Cl-(aq) => AgCl(s). L'équivalence est déterminée en mesurant la conductivité lors du titrage.
1) Définir l'équivalence et expliquer brièvement comment la déterminer.
B- Préparation de la solution à titrer
En septembre 2003, après un été caniculaire, on a prélevé un échantillon d'eau dans un marais salant de la zone prévue pour implanter l'élevage d'artémia. On dilue 10 fois cette eau pour obtenir la solution S1 à titrer.
2) On souhaite obtenir 50.0 mL de solution S1. Quel volume d'eau doit on prélever ?
3) Expliquer brièvement le mode opératoire.
C- Exploitation du dosage
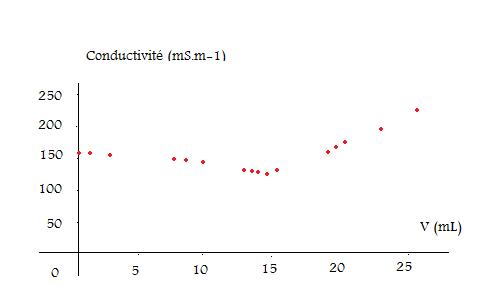
On réalise le titrage d'un volume V1= 10.0 mL de solution S1 par une solution S2 de nitrate d'argent de concentration apporté en soluté C2 = 1.00*10^-1 mol.L-1, et on trace l'évolution de la conductivité o (sigma) au cours du titrage en fonction du volume de nitrate d'argent versé.
4) a) Déterminer graphiquement le point d'équivalence E du dosage
b) Justifier sans calculs, la diminution de la conductivité avant l'équivalence
c) Justifier sans calculs, l'augmentation de la conductivité après l'équivalence
2) Déterminer la concentration molaire des ions Cl- dans la solution S1 et en déduire la concentration molaire des ions chlorure dans l'eau du marais. (on utilisera un tableau d'avancement)
3) Cette eau est elle favorabe au développement de Artémias ?
Données : Conductivité molaire ioniques à 25°C
Cl- : 7.63*10^-3 S.m².mol-1
Ag+ : 6.19*10^-3 S.m².ml-1
NO3- : 7.14*10^-3 S.m².mol-1
Na+ : 5.01*10^-3 S.m².mol-1
Merci de m'aider !! ^^
Oui pour le reste j'ai trouvé (enfin je crois ^^'')
Voici mes résultats :
B- 3/ il faut prélever 5mL de solution
C- 2/ concentration molaire des ions chlorure dans la solution S1 = 6.0*10^-1 mol.L-1
-------------------------------------------- le marais = 1.4 mol.L-1
bonjour,
j'ai le même devoir à faire pour demain, mais je galère pas mal!
je ne comprends pas comment Kakeru a fait pour la question B-3,on doit utiliser quelle formule ? C=n/V? Cm=m/V ? je m'embrouille un peu là :s
Bonjour, j'ai moi aussi ce type bac à faire pour mardi mais je ne comprend pas comment trouver 5mL pour 3-a. je fais calculs sur calculs et cela n'aboutit pas. comment avez vous fait?

 !
!
 )
)
