Inscription / Connexion Nouveau Sujet
Exercice structure chlorure de césium
Bonjour,
voilà, j'ai un dm de physique chimie à faire pendant les vacances ; ayant des difficultés cette année dans cette matière (un comble !) ma moyenne n'est pas très élevé... Bref je compte sur ce dm pour faire monter un peu ma moyenne.
C'est donc pour cela que je viens vous demander un peu d'aide.
J'ai effectué le premier exercice sans trop de soucis, mais le deuxième m'en pose un peu plus.
Plus précisèment, je ne suis vraiment pas certain de ce que j'ai fait.
Voici l'énoncé :
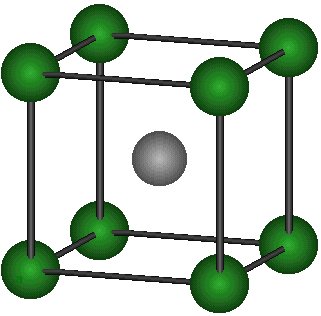
Le chlorure de césium est constitué d'ions césium Cs+ et d'ions chlorure Cl-. La structure de ce solide est schématisée ci-contre : c'est une structure cubique dans l'arête du cube est a=411pm
Les données : E=1,6.10-19 C ; k=9.109
Puis les questions :
A) D'après le schéma (voir bas de page), quelle est la distance qui sépare les deux ions chlorure les plus proches ?
J'en ai déduit qu'elle était de 411pm, la structure étant cubique, la distance la plus proche serait l'arête ?
B) Calculer la valeur de la force électrique entre ces deux ions. estèce une interaction attractive ou répulsive ?
J'ai posé le calcul Fe = (k.e²)/(d)²
-> Fe = 9.109
 ( 1,6.10-19 )2/(4,11.10-10)2
( 1,6.10-19 )2/(4,11.10-10)2
-> Fe = 1,36.10-9 N
Je pense qu'elle est répulsive car on parle de deux mêmes ions, donc de même signe.
Ma première difficulté arrive ici (à moins de m'être déjà trompé dans les deux premières questions) :
C) La longueur de la diagonale d'un cube d'arête a est : L= a.
 3
3
Quelle est la distance entre un ions Cl- est Cs+ ?
L'ions Cs+ semble être au centre du cube, la diagonale étant de a.
 3, je pense donc qu'il faut diviser la distance de cette diagonale par 2 ????
3, je pense donc qu'il faut diviser la distance de cette diagonale par 2 ????
L(diagonale)= a

 3
3
L(diagonale)= 411(pm)

 3
3
L(diagonale)= (4,11.10-10
 3 (en mêtre)
3 (en mêtre)
L(Cl-;Cs+)= 4,11.10-10

 3/(2)
3/(2)
L(Cs-;Cs+)= 3,56.10-10m
J'ai absolument besoin de cette valeur pour pouvoir continuer mon exercice, j'espere que vous allez pouvoir me confirmer (ou non) ce que j'ai fait ci-dessus.
Merci d'avance, Benj
Salut, tu as raison pour la question a.
Par contre tu t'es trompé. 1pm = 1^10(-12)m et non pas -10. Et c'est -1,6 car l'ion chlorure porte une charge négative (taurais le bon résultat puisque cest au carré mais situ as une prof casse couille, elle t enlèvera des points ^^)
ensuite ions de même charge donc tu as raison, c'est une interaction répulsive.
L'ion césium est situé au milieu du cube donc t'a raison, c'est la moitié de aracine3.
Mais tu as faux dans le calcul une nouvelle fois car 1pm = 1^10(-12)m
Salut Benj
Merci beaucoup ninipodchien ! Même si je dois avouer que j'ai rendu mon DM depuis quelque temps, faute de réponse...


