Inscription / Connexion Nouveau Sujet
exercice diagramme des niveaux d'energie de l'hydrogène
bonjour ! j'ai cet exercice à faire qui a été donné en tp je n'arrive pas a le faire est ce que quelque peut m'aider car la je bloque merci .
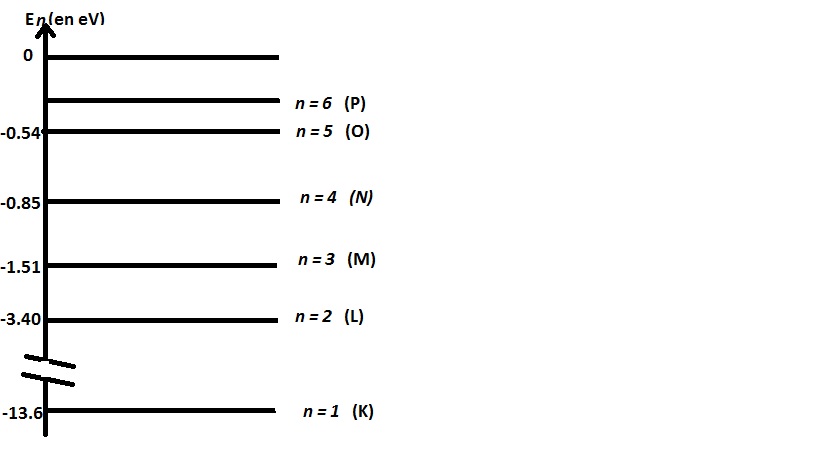
le diagramme d'énergie ci-contre représente les différents niveaux accessibles pour les électrons d'un atome d'hydrogène.
ces niveaux sont représentés par des lignes horizontales.
1) quelle énergie faut-il apporter à l'atome pour que son électron passe de la couche (K) à la couche (M)? exprimez cette énergie en électronvolts puis en joules.
2) quelle doit être la fréquence v de la radiation qui permet cette transition ?
3) une radiation de fréquence v' = 2v peut-elle être absorbée par cet atome ?
4) quelles transitions sont envisageables lorsque l'électron est sur la couche (M) et se désexite ?
5) déterminer la différence d'énergie entre la couche (L) et la couche (K).
6) en déduire la valeur de la longueur d'onde, dans le vide, du photon émis lors de la transition de la couche (L) à la couche (K). La radiation associée à ce photon appartient-elle au domaine du visible ?
données : *célérité de la lumière dqns led vide : C= 3.00*10^8 m.s^-1
*constante de Planck : h= 6.63*10^-34 J.s, 1eV = 1.602*10^-19J.