Inscription / Connexion Nouveau Sujet
Exercice de Phisique -chimie 1er S
Bonjour en effet je suis au CNED je suis en train de faire un devoir de phisique -chimie et j'aurais besoin d'aide 
voici l'énoncé
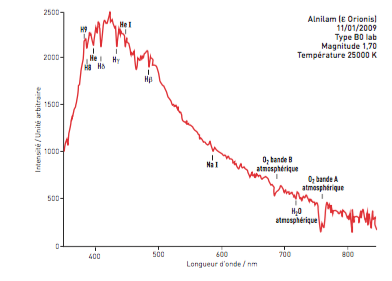
Interpreter le spectre de la lumiere d'une etoile. (6 points) Le profil spectral de l'etoile Alnilam est reproduit ci-dessous : voir image dans l'attachement
Le diagramme energetique simplifié de l'atome de sodium est reproduit ci-dessous.(aussi voir l'image )
----
Le niveau n = 1 est celui de plus basse energie.
On souhaite déterminer si la raie d'absorpointion notee Na I présente dans le spectre de l'étoile Alnilam correspond à une transition entre les niveaux 1 et 2 ou entre les niveaux 2 et 3 de l'atome de sodium.
1. Pourquoi dit-on que l'énergie d'un atome est quantifiee? (1 point)
2. La presence d'une raie d'absorpointion correspond-t-elle a une transition d'un niveau inferieur a un
niveau supérieur ou l'inverse ? (1 point)
3. Calculer les longueurs d'onde des photons correspondant à une transition entre les niveaux 1 et 2
d'une part et 2 et 3 d'autre part. (2 points)
4. A quelle transition correspond la raie notee Na I ? (1 point)
5. Que nous apprend la présence de cette raie au sujet de l'étoile Alnilam ? (1 point)
alors mois j ai fait just qu'au le n4
q 1 j ai repondue "l'atome n peut prendre que des niveuax d'energie bien determines (E1,E2,E3,E4.....) cela ilustre bien que l'energie de l'atome est quantifiee.
q 2
la presance d'un raie d'absorbtion correspond a une transition d'un niveau inferieur a un niveau superieur
Q3:
Niveau 1 et 2
E1=-5,14eV
E2= -3,03eV
DE=h*v <=> v=DE/h
(D c'est pour delta)
alors DE= Ep-En' avec Ep>En'
donc
DE=-3,03-(-5,14) = 2,11eV
l'atome gagne de l'energie en absorbant un photon
DE=h*c/lambda et on isole la longeur d'onde lambda
lambda= h*c/DE avec h= 6,626*10^-34 J.s
et c= 3,00*10^8m.S^-1
alors DE=2,11ev
= 2,11*1,602*10^-19= 3,38022*10^-19 J
donc lambda = 6,626*10^-34*3,00*10^8/3,38022*10^-19
= 5,8807*10^-7m
--
Niveau 2 et 3
E2=-3,03eV E3= -1,93eV
DE=Ep-En' avec Ep>En'
DE=(-1,93)-(-3,03) = 1,1 eV
DE=h*c/lambda <=> Lambda=h*c/DE
DE=1,1 ev ce qui fait 1,7622*10^-19J
et donc lambda = 6,626*10^-34*3,00*10^8/1,7622*10^-1 = 1,12802*10^-6
et pour Q 4 et 5 j 'arrive pas de trouver .... :\
SVP aidez moi et aussi je voudrais savoir si ce que j'ai deja fait est correct 
Merci d'avance de votre aide

Salut,
je n'ai pas vérifié tes calculs avec ma calculatrice, mais si tu as bien calculer c'est bon ( les calculs et valeurs sont bonne!)
Je vais maintenant te demander de convertir les lambda en nm.
Tu vois sur le spectre rouge que Na I correspond a un peux moins de 600nm ( a peux pres 580-590..).
Ainsi, une fois que tu aura convertis les lambda, tu tombe sur a peux près 600, ca va normalement tombé sur le passage du niveau 1 a 2, et tu en conclus que c'est cette transition qui correspond la raie Na I.
La lumière de l'étoile a donc traversé cette espece chimique, ce qui a conduit a une absorbtion ! Tu peux ainsi en conclure d'une présence de Na I au sein de cette étoile.
D'autres questions ? 
mkask je comprends pas tres bien quel lambda est a convertir ... ca sera egale a 588.06 nm la 1 et 2 ?
Et la redac je la fait comment ?
je veux dire nous avons 1,9878*10^-25/3,38022*10^-19 = la calculette me donne 0,00000058806 metres donc logiquement en nm c est 588,06? et pareil pour 0,00000112802 m = 1128.02 nm
comme t'a dit NI est dans le 1et 2 mais c est surtout a la redation que je pose question comme la faire au mieux ....
Bah oui, pourquoi vous traquaser vous la tete 
Lambda1=588 et lambda2=1128.
Redaction:
On observe que l'element Na I devrait correspondre a une transition valant plus ou moin 580nm.
En effet, nous avons vu que tel etais le cas pour la transition du niveau 1 au niveau 2
conclusion:
J'en conclus ainsi que ces cette transition qui correspond a l'absorbtion de Na I.
ok ?
redaction:
La lumiere provenante de l'etoile a forcement traversé cette element pour qu'il puisse etre absorbé
conclusion:
J'en conclus ainsi une presence de Na I au sein de cette etoile.
Tout simplement 
Q3:
[i]Niveau 1 et 2
E1=-5,14eV
E2= -3,03eV
DE=h*v <=> v=DE/h
(D c'est pour delta)
alors DE= Ep-En' avec Ep>En'
donc
DE=-3,03-(-5,14) = 2,11eV
l'atome gagne de l'energie en absorbant un photon
En revanche, je ne vois pas l'utilité de ce qui est marqué en rouge ?

 merci beaucoup
merci beaucoup 
