Inscription / Connexion Nouveau Sujet
Exercice 3 - Reprédentation de lewis (4 points) Molécule C2H5NO
Exercice 3 - Reprédentation de lewis (4 points)
On considère la molécule de formule brute C2H5NO.
1) Calculer le nombre de doublets liants et non liants de la molécule .(1 point)
2) Combien de liaisons covalentes ces atomes doivent-ils établir pour obtenir une structure électronique en duet ou en octet? (0,5 point)
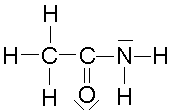
3) Ecrire la formule de Lewis possible (non cyclique) de cette molécule. (1 point)
4) Rappeler la définition de deux isomères. (0,5 point)
5) Ecrire la formule développée (ou semi-développée) de 2 autres isomères non cyclique de formule brute C2H5NO.(1 point)
Je n'arrive pas à faire cette exercice.
Quelqu'un aurais la gentillesse de m'aider s'il vous plait.
Merci
Bonjour shadowmiko,
La première page que tu m'as conseillé je suis déja aller la voir et la deuxième c'est en anglais ça ne m'aide pas
mais merci quand même.
Pour la question 3 et la question 4 j'y suis arrivée mais pas les autres.
1) écris les structures des atomes (premier lien) et ensuite tu fais les calculs classiques (nb d'éléctrons sur les couches externes etc.)
2) cite la règle et tu regardes vis à vis de ta première question
5) pour les isomères il te suffit de déplacer les doublets. Sur le O par exemple qui peut en porter 3. Et les C peuvent peut être faire des doubles liaisons. De même le O peut se lier à un H.
Bonjour, j'ai une question en physique que je n'arrive pas à répondre. Quelqu'un aurais la gentillesse de m'aider s'il vous plait.
Merci
Ecrire la formule développée (ou semi-développée) de 2 autres isomères non cycliques de formule brute C2H5NO. (1 point)
*** message déplacé ***
Bonjour shadowmiko,
je m'excuse d'avoir fait un multi-post je ne savais pas qu'on avais pas le droit.
Ca ne fait pas longtemps que je suis sur le site. Je serais pour la prochaine fois.
il me manque la question 5 mais je pense avoir une idée et la 1 j'ai trouver le nombre de doublets mais je ne sais pas combien il y a de doublets liants et non liants
Pour la représentation de Lewis tu dois :
# Calculer le nombre x d'électrons de la couche externe de chaque atome.
# Calculer le nombre y des doublets liants : y = x/2
# Calculer le nombre de doublets liants z : z = 2-1 = 1 pour l'hydrogène et z = 8 - q pour les autres atomes,q étant le nombres d'électrons de la couche externe de l'atome
# Calculer le nombre z' de doublets non liants.
z' = 0 pour l'hydrogène et z' = (q-z)/2 pour les autres atomes.
1)
Les doublets liants définis précédemment assurent les liaisons entre les atomes.
Les doublets non liants sont les paires d'électrons qui ne servent pas de liaisons entre deux atomes.
La représentation de la molécule de formule brute C_2 H_5 NO se fait en calculant préalablement le nombre de doublets d'électrons externes :
d= (2×4+5×1+1×5+1×6) / 2
d= (8+5+5+6) / 2
d= 24 / 2
d= 12 doublets.
y= x/2 = 24/2
Hydrogène : z=2-1=1
Carbone : z=8-4=4
Azote : z=8-5=3
Oxygène : z=8-6=2
Hydrogène : z'= (q-z)/2 = (1-1)/2 = 0
Carbone : z'= (q-z)/2 = (4-4)/2 = 0
Azote : z'= (q-z)/2 = (5-3)/2 = 1
Oxygène : z'= (q-z)/2 = (6-2)/2 = 2
J'ai fait ces calculs mais je ne sais toujours pas combien il y a de doublets liants et non liants sachant qu'il y en a 12 en tout.
L'hydrogène et le carbone ont 0 doublet non liants?
L'azote a 1 doublet non liants?
L'oxygène a 2 doublets non linats?
C'est çà ou pas.
Avec les pistes que tu m'as donné je n'y suis pas arriver.
Par contre j'ai trouver ca mais je ne suis pas sur du tout.
N-Méthylformamide : H3C-CH=N-O-H
L'acétaldéhyde oxime : CH3-NH-C=0
H

 !
!