Inscription / Connexion Nouveau Sujet
DM physique : l'atome de Rutherford
bonjour,
j'ai un dm de physique qui est assez compliqué
je vous donne mon probleme:
La structure lacunaire de la matière
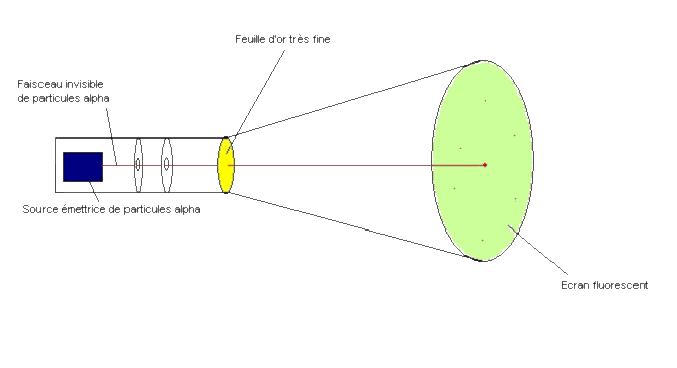
Description de l'expérience de Rutherford
En 1909, Marsden, Geiger et Rutherford entreprirent d'utiliser des particules (noyaux d'hélium), produites
lors de la désintégration de noyaux radioactifs de radium, pour explorer la structure de l'atome. Ils
bombardèrent pour cela une feuille d'or d'environ 0,6 m, placée dans une enceinte à vide, par une faisceau de
particules focalisées par deux diaphragmes D1 et D2.
Ils constatèrent que la grande majorité des particules traversent la feuille d'or sans être déviées. En effet, la
tache observée sur l'écran fluorescent garde la même intensité avec ou sans feuille d'or interposée. Quelques
particules sont légèrement déviées, comme en témoigne les impacts fluorescents sur l'écran.
Leur surprise fut de constater que certaines particules (une sur 20 à 30000) subissent de grandes déviations
(supérieures à 90 degrés) et sont donc renvoyées vers l'arrière.
Rutherford en déduisit (mais cela lui prit 2 ans de réflexion), que l'atome est constitué d'un noyau très petit par
rapport à la taille de l'atome et qui concentre l'essentiel de la masse et toutes les charges positives, et d'un
cortège électronique dont le volume est celui de l'atome.
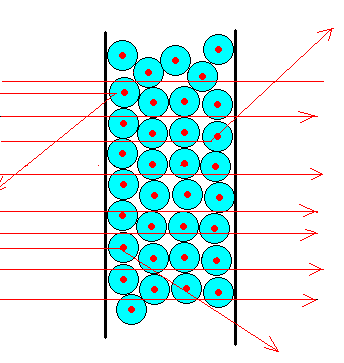
Interprétation de l'expérience de Rutherford
On considère le schéma ci-contre:
1,2,3,4,
13,14,15, représentent les
traces des particules lorsqu'elles
traversent la feuille d'or.
Questions
1. Que représentent les cercles en contact les uns avec les autres ?
2. Que représente le point au milieu de chaque cercle ?
3. Sachant que le rayon d'un atome d'or est de 0,144 nm et celui d'un noyau d'or est de 7 fm, quel est le
rapport des volumes du noyau et de l'atome ? Quel est le volume moyen occupé par un électron ?
4. Combien faut-il de couches d'atomes, empilées les unes sur les autres, pour obtenir une feuille d'or de 0,6
m d'épaisseur ? Le rayon d'un atome d'or est de 0,144 nm.
5. Quel est le rapport de la masse d'une particule à celle d'un électron ? Cela permet-il de comprendre
pourquoi la majorité des particules ne sont pas déviées ? On pourra s'aider de ce qui se passe lorsqu'une
boule de pétanque est lancée contre une balle de ping-pong.
6. Que se passe-t-il pour les particules 5, 9 et 14 ?
7. Lorsqu'une particule passe près d'un noyau, est-elle attirée ou repoussée par lui ? Sachant qu'une
particule porte une charge positive, que peut-on en déduire quant à la charge du noyau ?
8. Quel est le rapport de masse d'une particule à celle d'un noyau d'or ? Cela permet-il de comprendre
pourquoi les particules 5, 9 et 14 sont déviées ?
9. Comment peut-on expliquer que certaines particules soient renvoyées vers l'arrière ? Faire un schéma de
cette situation.
10. Choisir parmi les analogies suivantes, celle qui pour vous traduit le mieux l'expérience de Rutherford :
a) des joueurs de tennis qui envoient des balles contre un mur.
b) un enfant qui jette du sable à travers un grillage à larges mailles.
c) un chasseur qui tire des balles de chevrotine à travers une feuille de papier.
d) une planète bombardée par une pluie de météorites.
11. Que pensez-vous de la phrase de Rutherford : « il est aussi surprenant de voir des particules réfléchies
par une mince feuille d'or, qu'un boulet de canon renvoyé par une vitre » ?
12. Quelle est la masse volumique d'un noyau d'or ?
13. Une telle masse volumique se rencontre-t-elle ailleurs que dans les noyaux atomiques ?
14. Que pensez-vous de la phrase de Frédéric Joliot-Curie : « les noyaux de toute l'humanité, accolés,
occuperaient un volume inférieur à celui d'un dé à coudre » ? On admettra que tous les noyaux ont la
même masse volumique.
15. En quel sens peut-on dire que le remplissage de l'espace par la matière est lacunaire ?
merci de votre aide
1) je pense que la reponse est l'atome
2)le point au milieu de chaque cercle represente le noyau
meric de votre aide
3. Sachant que le rayon d'un atome d'or est de 0,144 nm et celui d'un noyau d'or est de 7 fm, quel est le
rapport des volumes du noyau et de l'atome ? Quel est le volume moyen occupé par un électron ?
pouver -vous m'aider sur cette question SVP.
pour un DM de 2dn c'est compliqué!
Je n'ai pas les compétences pour te répondre mais consulte les fiches de physiques, ça poura peut etre t'aider!
Bonsoir,
Ton sujet apparaît actuellement avec "7 réponses" et qui ne sont pas toutes de toi (sinon il apparaîtrait dans les sujets non répondus). Comme je n'interviens jamais quand quelqu'un d'autre répond je n'ai pas pensé que tu avais besoin d'aide. Par curiosité je suis venu lire ton sujet. Et pour ce soir je vais quitter l'
Mais s'il en est encore temps je t'aiderai dès demain.
Oui pour tes réponses aux questions 1 et 2
Question 3 : volume de deux sphères ; celle de rayon le noyau et celle de rayon l'atome ; rapport des volumes ; nombre d'électrons d'un atome d'or ; volume moyen occupé par un électron

Bonjour,
Je vais te donner des pistes de résolution. N'hésite pas à communiquer tes résultats ; je les vérifierai. Dis aussi si tu ne comprends pas quelque chose et que tu as besoin de plus d'explications.
Question 3 : voir mon précédent message
Question 4 : rayon de l'atome ; diamètre de l'atome ; épaisseur de la feuille 0,6 µm ; nombre d'atomes en supposant qu'ils s'alignent bien sagement
Question 5 : masse de l'électron (dans ton livre) ; masse d'une particule  : elle est dans ton livre ; sinon elle est à peu près (car il y a l'énergie de liaison) la somme des masses de ses constituants c'est-à-dire la somme des masses de deux protons et de deux neutrons c'est-à-dire de 4 "nucléons"
: elle est dans ton livre ; sinon elle est à peu près (car il y a l'énergie de liaison) la somme des masses de ses constituants c'est-à-dire la somme des masses de deux protons et de deux neutrons c'est-à-dire de 4 "nucléons"
Question 6 : je ne vois que 10 traces non numérotées... je suppose que "5, 9 et 14" correspondent à des particules plus ou moins déviées ; peux-tu expliquer pourquoi ?
Question 7 : une particule  : positive ou négative ? Donc le noyau de l'atome : positif ou négatif ?
: positive ou négative ? Donc le noyau de l'atome : positif ou négatif ?
Question 8 : combien de nucléons dans le noyau d'un atome d'or ? Dans celui d'un atome d'hélium (la particule  est un noyau d'atome d'hélium)... mais on a déjà vu ce nombre à la question 5 ? rapport des deux ? Conclusion ?
est un noyau d'atome d'hélium)... mais on a déjà vu ce nombre à la question 5 ? rapport des deux ? Conclusion ?
...
Question 12 : masse d'un noyau d'or ; volume de ce noyau (déjà calculé à la question 3) ; masse volumique (écriture scientifique indispensable...)
...
A toi. Je suivrai ta progression

3) la formule pour trouvé une aire est (V = 4/3 p R au cube)
volume du noyau: 4/3 p 7 au cube = 1436 fm
volume de l'atome : 4/3 p 0.144 au cube = 12507 fm
on fait pour trouver le rapport: 12507/1436 = 8.7
le rapport des volumes du noyau et de l'atome est de 8.7
pour trouver le volume d'un electron on fait: 12507-1436= 11071
le volume d'un electron est de 11071 fm cube.
je ne suis pas sur
Bonsoir,
Le fermi ou femtomètre est une unité de longueur (pas une unité de volume)
1 fm = 10-15 m
le nanomètre est aussi une unité de longueur (toujours pas de volume)
1 nm = 10-9 m = 1 000.10-12 m = 1 000 000.10-15 m
c'est-à-dire
1 nm = 1 000 pm = 1 000 000 fm
Donc le rayon de l'atome d'or est de 0,144 nm = 144 pm = 144 000 fm
D'accord avec ton calcul du volume du noyau : 1 437 fm3 (fermi cube ou femtomètre cube)
Mais il faut que tu recommences le calcul du volume de l'atome
Enfin pour le volume moyen occupé par un électron il faut d'abord se poser la question du nombre d'électrons autour d'un noyau d'or. Combien un atome d'or a-t-il d'électrons (à l'état neutre) ? Pour le savoir : un coup d'il sur ta table des éléments (tableau de Mendéléiev)

1 fm = 0.001 pm = 0.000001 nm
volume de l'atome : 4/3 p 0.144 au cube = 0.6031857895 nm cube = 6 * 10 puissance 17 fm cube
est-cela?
Non, tu as oublié d'élever 0,144 au cube
Si on note le volume de l'atome en nm3
et en effet il faudra multiplier par 1018 pour exprimer ce même volume en fm3

volume de l'atome = [u]1.25 *10[/sup]16 fm[sup]3
ensuite il faut diviser volume de l'atome par le volume du noyau:
(1.25 *10[sup][/sup]16)/ 1437 = environ 8.7
Quel est le volume moyen occupé par un électron ?
je ne sais pas puisque l'on nous dit pas le nombre d'electrons ni leur rayon
Bonjour POU60,
Oui pour le volume de l'atome : c'est bien 1,25.1016 fm3
Comme le volume du noyau est 1 437 fm3
le rapport des deux est 1,25.1016 / 1 437 = 8,7.1012
Il ne faut pas oublier le coefficient 1012 sinon on se trompe d'un coefficient qui vaut un million de millions (ou mille milliards)... c'est quand même une "grosse" erreur...
Il me semble bien si tu as copié en entier ton énoncé et toutes les valeurs numériques qui l'accompagnent qu'il te manque des données (plusieurs) : il te faut peut-être les chercher dans ton livre car ce sont toutes des données qui s'y trouvent à de nombreuses reprises. Je vais t'aider :
l'or est le 79e élément du tableau de Mendéléiev, cela signifie qu'il a 79 protons et, s'il est neutre, c'est-à-dire s'il n'a pas perdu ses électrons par ionisation, qu'il a également 79 électrons.
Tu peux négliger le volume d'un électron de même que tu peux négliger le volume du noyau (tu as vu à quel point il est extrêmement petit par rapport au volume de l'atome). Donc pour terminer la question 3 il te suffit de diviser le volume de l'atome (1,25.1016 fm3) par 79 qui est le nombre d'électrons.
Pour la question 4 :
tu me confirmeras que l'épaisseur de la feuille d'or est 0,6 µm (dans l'expérience des élèves de Rutherford, Hans Geiger et Ernest Marsden, ils ont utilisé des feuilles 10 fois plus minces soit 0,06 µm ou 60 nm)
Tu connais le rayon de l'atome, donc son diamètre. Combien faut-il mettre de diamètres bout à bout pour atteindre l'épaisseur de la feuille ?
Pour la question 5 :
masse d'un électron : 9,109.10-31 kg
masse d'une particule  : 6,666.10-27 kg
: 6,666.10-27 kg
A toi...

3) (1,25.1016) / 79 = 1.58*1014
le volume moyen occupé par un électron est de 1.58*1014
4) l'épaisseur de la feuille d'or est bien de 0,6 µm
le diametre de l'atome = 0.288 nm
1 µm = 1000 nm
0,6 µm = 600 nm
il suffit de faire 600/0.288 = environ 2083il faut 2083 couches d'atomes pour obtenir une feuille d'or de 0,6
µm d'épaisseur
Oui !
Tes résultats numériques sont bons.
ATTENTION : n'oublie jamais les unités en physique.
Volume moyen occupé par un électron : 1,58.1014 fm3
Oui, un peu plus de 2 000 atomes dans l'épaisseur de la feuille d'or, ce qui est assez peu (à cette épaisseur l'or est transparent, comme à travers une vitre de couleur verte).

je sais que la masse d'un électron : 9,109.10-31 kg
mais comment tu a trouvé que la masse d'une particule : 6,666.10-27 kg
merci
J'ai pris un livre...
Tu peux avoir une approximation suffisante en disant qu'une particule  c'est un noyau d'hélium et en faisant la somme des masses des particules qui composent ce noyau.
c'est un noyau d'hélium et en faisant la somme des masses des particules qui composent ce noyau.
Le noyau d'hélium (l'hélium est le deuxième élément du tableau de Mendéléiev) a deux protons ; il a aussi deux neutrons ; son numéro atomique est Z = 2 (nombre de protons) et son nombre de masse est A = 4 (somme des protons et des neutrons) donc son nombre de neutrons est N = A - Z = 4 - 2 = 2
Tu additionnes la masse de deux neutrons plus la masse de deux protons et tu trouves environ 6,69.10-27 kg
ce n'est pas tout à fait la masse du noyau qui est toujours plus léger que la somme des masses de ses constituants (c'est l'énergie de liaison ; et comme E = m.c2 cette énergie libérée à la constitution du noyau c'est de la masse perdue on l'appelle le "défaut de masse" ; mais je crois que ce n'est pas encore à ton programme si tu es vraiment en 2nde).
La "vraie" masse de la particule  est un peu plus faible que 6,69.10-27 kg c'est 6,67.10-27 kg ; mais tu vois que pour la question qui t'est posée cela n'a guère d'importance.
est un peu plus faible que 6,69.10-27 kg c'est 6,67.10-27 kg ; mais tu vois que pour la question qui t'est posée cela n'a guère d'importance.

merci de ton aide
5)on fait 9,109.10-31 kg / 6,666.10-27 kg = 1.37*10-4
le rapport de la masse d'une particule à celle d'un électron est de 1.37 * 10-4
Cela permet de comprendre pourquoi la majorité des particules ne sont pas déviées
6) les particules 5, 9 et 14 sont déviées par le noyau de l'atome d'or puisqu'il n'y a qu'eux qui sont en contact avec le noyau et comme la masse des particules est faible par rapport a la masse du noyau alors seul les particules sont déviée
Lorsqu'une particule passe près d'un noyau,elle est attirée par lui car la particule porte une charge positive, le noyau est aussi une charge positives car une charge negative est attiré par une charge positive

Très bien !
Une particule  est environ 7 300 fois plus massive qu'un électron. Les nuages d'électrons autour des noyaux ne l'empêchent donc quasi pas de passer en ligne droite.
est environ 7 300 fois plus massive qu'un électron. Les nuages d'électrons autour des noyaux ne l'empêchent donc quasi pas de passer en ligne droite.
Parfois, mais c'est très rare car tu as vu comme un noyau est incroyablement petit par rapport à l'atome, une particule  s'approche d'un noyau et là elle est déviée car les charges positives (les 2 protons) de cette particule sont repoussées par les charges positives (les 79 protons) du noyau d'or. Il vaut mieux ne pas parler de "contact" : il n'y a pas contact. Comme le noyau d'or est très lourd par rapport à la particule il ne bouge quasi pas, c'est la particule qui est déviée.
s'approche d'un noyau et là elle est déviée car les charges positives (les 2 protons) de cette particule sont repoussées par les charges positives (les 79 protons) du noyau d'or. Il vaut mieux ne pas parler de "contact" : il n'y a pas contact. Comme le noyau d'or est très lourd par rapport à la particule il ne bouge quasi pas, c'est la particule qui est déviée.

8)masse d'une particule : 6,666.10-27 kg
masse du noyau d'or : 1,67 * 10-27 kg
on fait: (6,666.10-27) / (1,67 * 10-27)
= 3.99
Cela ne permet pas de comprendre pourquoi les particules 5, 9 et 14 sont déviées car la masse de la particule est superieur a la masse du noyau

Ça c'est la masse d'un noyau d'hydrogène : un seul proton
Non, la masse d'un noyau d'or... combien de "nucléons" (protons + neutrons) dans un noyau d'or. Tu connais déjà le nombre de protons, c'est 79 ; combien de neutrons ? Ou encore, quel est le nombre de masse (A) d'un noyau d'or. La nombre de neutrons sera N = A - 79
Ensuite la masse du noyau d'or sera voisine (un peu inférieure) à la somme des masses des 79 protons et des ... neutrons.
D'accord ?

noyau d'un atomme d'or :
son numéro atomique est Z = 79 (nombre de protons) et son nombre de masse est A = 197 (somme des protons et des neutrons) donc son nombre de neutrons est N = A - Z = 197 - 79 = 118
118 (1.67*10-27) + 79 (1.67*10-27)
= 3.3 * 10-25
pour touver le rapport on fait:
(3.3 * 10-25) / (6,666.10-27)
= 49.5
Cela permet de comprendre pourquoi les particules 5, 9 et 14 sont déviées car la masse de la particule est tres largement infeieur a la masse du noyau
10) celle qui traduit le mieux l'experience de rutherford est la b)un enfant qui jette du sable à travers un grillage à larges mailles.
11) je pense que sa veut dire qu'il n'y a aucune chance de voir des particules réfléchies par une mince feuille d'or
question 10 : d'accord avec toi : la probabilité que du sable revienne en arrière est très faible si le grillage est à larges mailles. L'essentiel passera sans être dévié
question 11 : Cette phrase exprime l'extrême surprise de Rutherford. Avant cette expérience on imaginait l'atome comme un nuage de particules négatives et positives : il n'y avait aucune possibilité qu'en envoyant une particule  plus lourde que ces particules et avec une grande vitesse elle puisse revenir en arrière ! Et pourtant c'est ce qui a été observé ! Donc il a fallu changer de modèle et Rutherford a imaginé qu'il y avait dans chaque atome un noyau capable de concentrer la charge électrique positive (dans un premier temps il n'avait pas imaginé qu'il y avait toute la charge électrique mais seulement la moitié ; ne tiens pas compte de ce que je te dis là... c'est pour ta culture) et aussi capable de concentrer la masse ; et il fallait que le noyau soit très petit parce que la quasi totalité des particules
plus lourde que ces particules et avec une grande vitesse elle puisse revenir en arrière ! Et pourtant c'est ce qui a été observé ! Donc il a fallu changer de modèle et Rutherford a imaginé qu'il y avait dans chaque atome un noyau capable de concentrer la charge électrique positive (dans un premier temps il n'avait pas imaginé qu'il y avait toute la charge électrique mais seulement la moitié ; ne tiens pas compte de ce que je te dis là... c'est pour ta culture) et aussi capable de concentrer la masse ; et il fallait que le noyau soit très petit parce que la quasi totalité des particules  passaient sans être déviées.
passaient sans être déviées.
Question 12 : la masse volumique... attention, énorme surprise...

c'est bon j'ai trouvé:
volume du noyau :1436 fm
masse volumique kg fm-3 = masse (kg)/ volume (fm3)
(1,67 * 10-27) / 1436 fm3
= 1.16 * 10-30fm3
la masse volumique du noyau est de 1.16 * 10-30fm3

Tu as refait une erreur déjà faite plus haut : en prenant une masse de 1,67.10-27 kg pour masse du noyau tu fais comme si le noyau de l'atome d'or ne contenait qu'un seul nucléon. Or tu as trouvé qu'il en contient 197 donc la masse volumique est 197 fois plus grande
c'est-à-dire environ 2,3.10-28 kg.fm-3
et comme 1 fm = 10-15 m on a 1 fm3 = 10-45 m3
c'est-à-dire que la masse volumique du noyau est environ de 2,3.10-28.1045 = 2,3.1017 kg.m-3
C'est un nombre ahurissant ! Tu peux faire différentes conversions et tu trouves une masse volumique, par exemple, de 230 000 tonnes pour 1 mm3...
Voilà qui va te servir pour la fin du problème

14) cela veut dire que les noyaux sont tellement petits qu'il occuperaient un volume inférieur à celui d'un dé à coudre s'il sont tous reunit.
par contre on ne peut meme pas imaginer l'enorme masse volumique qu'elle contiendrait.
De plus cela prouve qu'il n'y a presqu'aucune chance de voir des particules réfléchies par une mince feuille d'or
Bonjour,
Schéma pour la question 9 : c'est cela ; ou bien la particule arrive vraiment avec une direction qui la ferait passer par le centre d'un noyau et alors elle est renvoyée vers l'arrière (encore une fois cette probabilité est très petite quand on considère le minuscule volume du noyau) ; ou bien elle passe loin d'un noyau et continue tout droit (parfois en perdant un peu d'énergie si elle arrache un électron à son atome au passage) ; parfois elle passe près d'un noyau et est déviée.
Comment l'expliquer ? La particule  est chargée positivement (deux protons) et le noyau est lui aussi chargé positivement (79 protons pour le noyau d'or) : plus la particule
est chargée positivement (deux protons) et le noyau est lui aussi chargé positivement (79 protons pour le noyau d'or) : plus la particule  s'approche d'un noyau et plus les forces de répulsion électrostatiques sont importantes (elles varient en raison de l'inverse du carré de la distance ; deux fois plus près = quatre fois plus repoussé, etc.) ; comme le noyau est lourd il ne recule presque pas, c'est la particule
s'approche d'un noyau et plus les forces de répulsion électrostatiques sont importantes (elles varient en raison de l'inverse du carré de la distance ; deux fois plus près = quatre fois plus repoussé, etc.) ; comme le noyau est lourd il ne recule presque pas, c'est la particule  qui fait demi-tour (encore une fois sans contact ; sinon, si la particule a une vitesse, donc une énergie, suffisante, ce qui n'est pas le cas ici, elle entre dans le noyau et il y a alors une "réaction nucléaire")
qui fait demi-tour (encore une fois sans contact ; sinon, si la particule a une vitesse, donc une énergie, suffisante, ce qui n'est pas le cas ici, elle entre dans le noyau et il y a alors une "réaction nucléaire")
Question 14 : quand Frédéric Joliot-Curie a prononcé cette phrase l'humanité ne comportait pas encore 6 milliards de personnes. Mais on va quand même actualiser le calcul.
Supposons (chiffre utilisé par les compagnies aériennes) qu'une personne ait une masse moyenne de 77 kg. 6.109 personnes ont donc une masse de
M = 6.109 * 77 = 4,6.1011 kg
Tu connais la masse volumique de la matière dans un noyau :

 2,3.1017 kg.m-3
2,3.1017 kg.m-3
donc le volume qu'occuperait une humanité "compactée" à la masse volumique des noyaux serait
V = M /  = 4,6.1011 / 2,3.1017
= 4,6.1011 / 2,3.1017  2.10-6 m3 = 2 cm3
2.10-6 m3 = 2 cm3
ce qui est bien le volume d'un dé à coudre...
Question 15 : imagine maintenant le volume qu'occupe vraiment 6 milliards de personnes... La différence entre ce volume et celui d'un dé à coudre est faite du vide qu'il y a dans chaque atome. La matière est vraiment très lacunaire (cherche ce mot dans un dictionnaire).

merci de ton aide,sans toi je pense que je serait toujours a la question 3
je te remercie encore et longue vie a l'ile des maths
Quel est le volume moyen occupé par un électron ?
on a trouvé :Volume moyen occupé par un électron : 1,58.1014 fm3
mais ce resultat c'est le volume moyen occupé par tous les electrons.
Puisque l'atome d'or a 79 electrons, je pense qu'il faut diviser 1,58.1014 fm3 par 79 = 2.1012
Volume moyen occupé par un électron est de 2.1012
merci



