Inscription / Connexion Nouveau Sujet
DM Oxydant/reducteur
On plonge une lame de zinc dans un V=100ml d'une solution de nitrate d'argent Ag++NO-3, de concentration C=0.10mol.L-1. Les ions argent réagissent avec le métal zinc pour donner un dépot d'argent métallique et des ions zinc (II) Zn2+.
1) quels sont les couple oxydant/reducteur mis en jeu ?
2)ecrire l'équation de la reaction
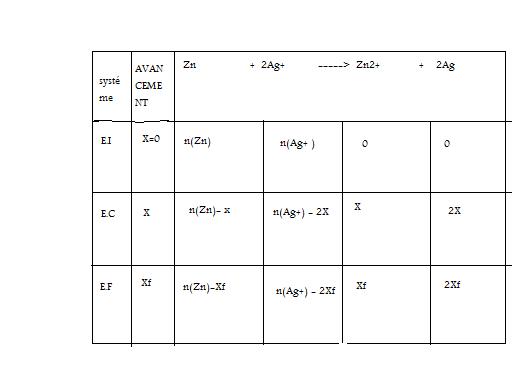
3) compléter un tableau d'avancement
4)le zinc étant en exés, quelle est la masse d'argent déposée en fin de réaction ?
5) quelle est alors la masse de zinc consommée ?
J'ai répondu au 3 er question qui me donne sa :
1) Zn2+/Zn
Ag+/Ag
2) Zn + 2Ag+ -----> Zn2+ + 2Ag
3) Voir l'image attaché.
je ne sais pas comment faire pour la 4 peut-on m'expliquer ?? =)
Vous pouvez aussi verifier si mes premiere réponse sont juste ? Svp =)
Un réactif en excès n'est pas entièrement consommé au cours de la réaction. donc celà signifie que l'argent est le réactif limitant.Tu peux en déduire ainsi la réponse à ta question .
ok enféte je calcule Xf de Ag+ puis j'utilise la formule n=n/M ==>
m= n*M =)
merci
mais comment peut on calculé la masse de zinc consommée si on a pas sa masse du départ ?




