Inscription / Connexion Nouveau Sujet
DM de Chimie 4
SVP pouvez vous m'aider pour cet exo :
1) On mélange 200mL de solution de chlorure de potassium à 5,0.10^-3 mol/L er 800ml de solution de chlorure de sodium à 1.25.10^-3 mol/L. Quelle est la conductivité de la solution obtenue?
2) Dans le mélange pécédent, on place la cellule d'un conductimetre. La surface des électrodes est de 1.0 cm² et la distance les séparant de 1.1 cm. Quelle est la valeur de la conductance indiquée par le conductimetre ?
Merci
Bonjour,
le volume total de la solution est V = 200 + 800 = 1000 mL = 1 L
Solution 1
V1 = 200 mL
C1 = 5,0.10-3 mol/L
donc [K+] = [Cl-]1 = C1
tu peux calculer les quantités de matière de K+ et Cl- :
* n(K+) = [K+].V1 = .....
* n1(Cl-) = ....
Solution 2
V2 = 800 mL
C2 = 1,25.10-3 mol/L = C2
de même [Cl-]2 = [Na+] = C2
tu peux calculer les quantité de matière de Na+ et Cl-
* n(Na+) = [Na+].V2 = .....
* n2(Cl-) = [Cl-]2.V2 = ......
Donc dans la solution finale S, tu peux calculer les nouvelles concentrations avec le volume V cette fois-ci (f pour final)
* [K+]f = n(K+)/V = ....
* [Cl-]f = ( n1(Cl-) + n2(Cl-) )/V = ....
* [Na+]f = n(Na+)/V
Finalement la conductivité vaut
 =
= 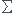
 k.[X]fk
k.[X]fk
2. C'est du cours.
Voir la fiche Rappels de chimie dans la section terminale si tu as un doute


