Inscription / Connexion Nouveau Sujet
DM Caféine
Salut, donc j'ai un DM sur des documents à rendre demain, j'ai déjà fais les 6 questions mais je ne sais pas comment faire la septième question et la résolution de problème. Voici l'énoncé :
La caféine, contenue dans les grains de café, est une espèce chimique qui agit comme un excitant.
Plus la teneur en caféine d?une tasse de café est importante, plus l?excitation du consommateur sera grande. Il est recommandé de ne pas dépasser une consommation quotidienne de caféine de 600 mg/jour pour éviter un état de surstimulation du système nerveux (excitation, insomnie, anxiété, troubles gastro-intestinaux, ...) 
Le but de l?exercice est de déterminer la concentration en caféine d?une tasse de café expresso grâce à un dosage par étalonnage utilisant la spectrophotométrie UV-visible.
Une solution de caféine de concentration massique Cm0= 3,2 g.L
-1est préparée à partir de caféine purifiée dissoute dans du dichlorométhane
. Elle va servir à préparer des solutions étalons de concentrations massiques:
0,40 g.L-1, 0,80 g.L-1, 1,2 g.L-1et 1,6 g.L-1.
Matériel à disposition:
Béchers de 100 mL et 200 mL
; fioles jaugées de 50,0 mL et 100,0 mL; pipettes jaugées de 10,0 mL et 25,0 mL; éprouvette graduée de 25 mL.
Les absorbances des cinq solutions étalons de caféine ont été mesurées
à ? = 271 nm:
Cm(en g.L-1) A
0,40 0,12
0,80 0,24
1,2 0,40
1,6 0,5
3,2 1,00
Dans les mêmes conditions, l?absorbance de la tasse de café
expresso a été mesuré: A = 0,61
Questions préliminaires:
1.La caféine est-elle une molécule organique? Justifier.
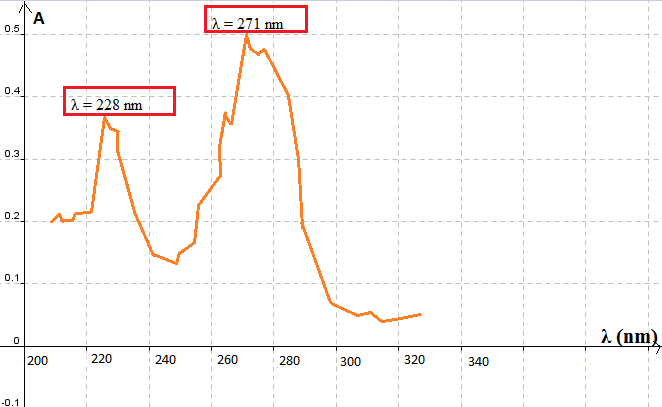
2.A l?aide du spectred?absorption, déterminer si une solution de caféine est colorée ou incolore.
3.Le résultat était-il prévisible à partir de la formule de la molécule? Justifier.
4.Parmi le matériel à disposition, indiquer celui utilisé pour préparer la solution de caféine de concentration massique Cm= 0,80 g.L-1. Justifier votre choix.
5.Pourquoi avoir choisi comme longueur d?onde d?étude ? =271 nm?
6.Quelle loi relie l?absorbance A à la concentration molaire C?
7.L?absorbance est-elle aussi proportionnelle à la concentration massique Cm? Justifier.
Résolution de problème:
Combien de tasses de 50 mL de ce café expressopeut-on boire par jour?
Voila mes réponses :
1) Elle est une molécule organique car elle possède un grand nombre d'atome de carbone et d'hydrogène. Ils sont liés entre eux ce qui forme la chaine carbonné.
2) La solution est incolore car elle absorbe dans l'ultraviolet
3) Le résultat était prévisible car elle possède seulement 3 liasons doubles conjugués donc pas un grand nombre de liaisons double conjugués.
4)Pour effectuer une dilution il faut utiliser du materiel jaugé de mainère à être le plus précis possilbe. On determine d'abord le facteur de dilution qui permet de déterminer le rapport entre le volume de la fiole jaugée et de la pipette jaugée.
Cmère/Cfille=3,2/0.8=4 et Vfiole/Vpipette= 100/25=4
On choisis donc la pipette jaugée de 25mL et la fiole jaugé de 100mL et de la pipette.
5) On travail à la longuer d'onde où l'absorbance est maximal pour avoir la meilleur précision donc 271nm.
6) La loi qui relie l'absorbance A à la concentration A à la concentration molaire C est la loi de Beer-Lamber : K=A/C 3,2/1= 3,2
Après j'arrive pas surtout le passage avec la concentration massique. Pouvez vous m'aider svp.
***Images ajoutées --> il y a un bouton pour cela : "Img"***
Bonjour.
Tout est correct sauf votre calcul de la question 6)...
6) La loi qui relie l'absorbance A à la concentration A à la concentration molaire C est la loi de Beer-Lamber : K=A/C 3,2/1= 3,2
 K = 1 / 3.2
K = 1 / 3.2  0.31 L/g.
0.31 L/g.
Pour la dernière question, Cmolaire = Cmassique / M.
Tirez Cmassique de cette relation et remplacez la dans l'expression de la loi de Beer-Lambert.
Calculez la masse molaire M de la caféine et exprimez finalement A en fonction de Cmolaire.
A plus.