Inscription / Connexion Nouveau Sujet
dm
Bonjour, voici un exercice , pouvez vous m'aider svp ?
Dans un flacon fermé de 200mL relié à un pressiomètre , on fait réagir 40 mL d'acide chlorydrique de concentration 1.00 mol.L avec un morceau de calcaire de mase m=8.50 g. L'équation de la réaction s'écrit :
2 H + + CaCO3 -> CA 2+ + CO2 + H2O
On estime que la température reste contante au cours de la réaction à 25 °C
1.a Quelle est la pression de départ dans le flacon ?
1.b Faire un shéma annoté du dispositif expérimental .
1.c Commen va évolur l pression dans le flacon en fonction de l'avancement de la réaction? POURQUOI?
2.A Déterminer les quantits de matieres des reactifs
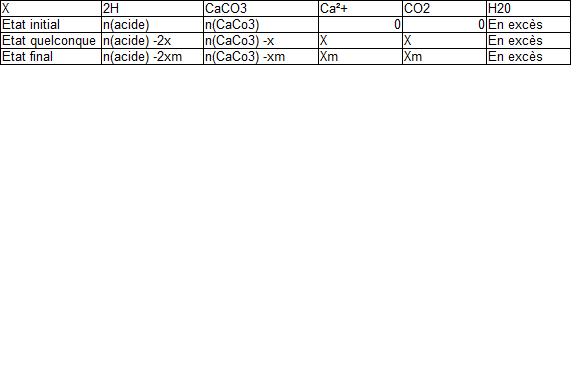
2.B Elaborer le tableau d'avancement de la réaction
2.C Quel est le réactif limitant?
3.a Sachant qur la tubulure reliant le flacon au pressiomere a un volume negligeable , calculer le volume occupe par le gaz dans le flacon
3.B on considérera le dioxye de carbone comme un gaz parfait . Trouver l'espression litterale de la pression en dioxyde de carbone Pco2 dans le flacn . Calculer cette pression en Pascal puis la convertir en hectopascal (hPa)
Merci beaucoup
1.a utilise la formule P*V=n*R*T (oublie pas de mettre T en kelvin!)
c Je dirai que la pression va augmenter car c'est souvent le cas mais je nai pas de justification
2.a c=n/v donc n=c*v tu as alors n(acide)=1.00*40*10^-3 = 40.10^-3 mol
1.a utilise la formule P*V=n*R*T (oublie pas de mettre T en kelvin!)
c Je dirai que la pression va augmenter car c'est souvent le cas mais je nai pas de justification
2.a c=n/v donc n=c*v tu as alors n(acide)=1.00*40*10^-3 = 40.10^-3 mol
pour n(CaCO3) tu fai n=m/M m=8.50g et M tu doi le calculer en ajoutent M(Ca)+3M(C)+3M(O)
c
pr le réactif limitant tu calcule n(acide)-2xm=0 et n(CaCO3)-xm=0
tu resouds les 2 equations et celle qui a le resultat le plus petit correspond a ton réactif limitant
b