Inscription / Connexion Nouveau Sujet
devoir maison chimie
bonjour j'ai un devoir maison a finir je l'ai commencé mais je bloque sur une question alors voici l'énoncé et la question qui me coince:
l'acide ascorbique de formule brute C6H8O6 appelé vitamine C est vendu sous forme de sachets contenant une poudre orangée essentiellement constitué d'acide ascorbique. Le but de l'exercice est de déterminer la masse d'acide ascorbique présente dans un sachet. Pour cela on effectue les opérations suivantes:
- on dissout un sachet de vitamine C dans 250 ml d'eau distillée pour obtenir la solution S.
- on dose par titrage la totalité de la solution S par une solution d'hydroxyde de soduim de concentration Cb=0.32mol.L
le titrage est suivi par conductimétrie et on obtient un graphe (elle donne une courbe montante a partir de 10 ml) représentan l'évolution de la conductance G en fonction du volume Vb d'hydroxyde de sodium ajouté.
la première question était: quelle est la formule de la base conjuguée de l'acide ascorbique?
j'ai répondu:C6H8O6/C6H7O6 et H2O/HO- (si ce n'est pas la bonne réponse vous pouvez m'aider également)
la deuxième question était:ecrire l'équation de la réactionentre l'acide ascorbique et les ions hydroxyde.
j'ai répondu: C6H8O6  C6H7O6 + H+
C6H7O6 + H+
HO- + H+  H2O
H2O
le résultat est C6H8O6 + HO-  C6H7O6 + H2O (c'est le résultat de la réaction)
C6H7O6 + H2O (c'est le résultat de la réaction)
la troisième question c'est celle ou je bloque qui est: dresser le tableau d'évolution du titrage. A l'équivalence on note Xe la valeur de Xmax à l'équivalence.
je ne sais vraiment pas comment faire ce genre de tableau. On me dit que c'est comme un tableau d'avancement mais ça non plus jassimile pa encore j'aimerais vraiment que quelq'un m'aide au plus vite
merci d'avance.
PS: le DM est a remettre lundi13 déc.
Bonjour.
Q1) Base conjuguée de l'acide ascorbique
Il s'agit de l'ion ascorbate de formule C6H7O6(-)
(Attention à ne pas oublier la charge de l'ion sinon vous ne respectez pas l'électroneutralité de la solution !)
Q2) Réaction avec la soude
Comme signalé au-dessus, l'équation acido-basique correcte (respectant la conservation de la charge) est :
C6H8O6  C6H7O6(-) + H(+)
C6H7O6(-) + H(+)
Et du coup,
C6H8O6 + HO(-)  C6H7O6(-) + H2O
C6H7O6(-) + H2O
Q3) Evolution du dosage
Vous allez devoir vous replonger intensément dans les cours de 2nde donc !
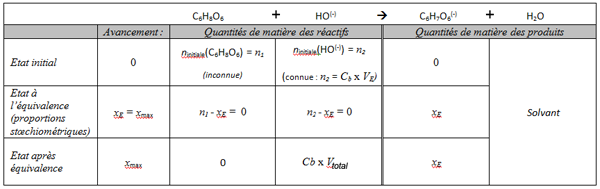
Voici un tableau d'avancement (ou de titrage) de votre réaction qui devrait sensiblement correspondre à ceux dont vous avez l'habitude de voir.
Dedans, on y inscrit TOUTES les quantités de matières lors de la réaction.
- sauf erreur de ma part -