Inscription / Connexion Nouveau Sujet
devoir maison !
bonjour à tous !
j'ai besoin de votre aide pour un exercice , veuillez m'aider svp !!
objectif : être capable d'identifier chaque famille de biomolécule a partir de la formule d'une molécule . Reperer les liaisons hydrolysables et écrire les réactions d'hydrolyse
parmi les molécules suivantes :
1) identifiez les fonctions caractéristiques et en déduire la nature de chacune de ces molécules
2) entourer les liaisons hydrolysables
3) pour chaque molécule écrire la réaction d'hydrolyse
je vous met les molécules en pièces jointes ( pour la molécule de pentapeptide je n'arrive pas a la mettre elle est trop grande )
pour la molécule d'oléine à la fin au lieu de : C8H17 c'est ( CH2)7-CH3
j'ai besoin de votre aide pour un exercice , veuillez m'aider svp !!
objectif : être capable d'identifier chaque famille de biomolécule a partir de la formule d'une molécule . Reperer les liaisons hydrolysables et écrire les réactions d'hydrolyse
parmi les molécules suivantes :
1) identifiez les fonctions caractéristiques et en déduire la nature de chacune de ces molécules
2) entourer les liaisons hydrolysables
3) pour chaque molécule écrire la réaction d'hydrolyse
QUESTION 1 :
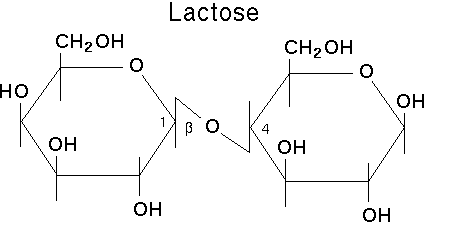
molécule de lactose : Le lactose est un diholoside composé d'une molécule de galactose et d'une molécule de glucose reliées entre elles par une liaison osidique .
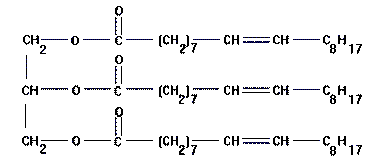
molécule d'oléine : l'oléine est un triglycéride formées de 3 fonctions ester et de l'association d'un alcool le glycérol et de 3 acides gras ( acide oléique)
molécule de pentapeptide : constitués de 4 fonctions amides et d'acides aminés qui résulte d'un peptide
QUESTION 2 :
molécule pentapeptide : j'ai entouré les CH2OH , les CH2
molécule de lactose : j'ai entouré les CH2OH
molécule d'oléine : j'ai entouré les CH2
QUESTION 3 :
molécule 1 : j'ai pas trouvé l'equation d'hydrolyse aidez moi svp !
molécule 2 : C12 H22 O11 + H2O ----> C6 H12 O6 + C6 H12 O6
molécule 3 : j'ai trouvé C57H104O6 + 3H2O ---> C3H8O3 + 3 C18H34O2
bonjour,
je ne suis pas très calé en biochimie,mais je peux essayer de t'aider.
dans la question 1 ,on demande d'identifier des fonctions chimiques (comme fonction alcool,aldéhyde , amine,amide acide .. ...)
dans le cas de la molécule de lactose ,il y a surtout des fonctions acool,une fonction hémiacétal dans l'ose de droite ,et une liaison osidique qui relie les 2 oses.
Pour l'ose de gauche ,sa fonction hémicétalique a été engagée pour participer à la formation de la liaison osidique .
on peut dionc identifier un diholoside réducteur car une fonction hémiacétal reste libre.
A toi de faire le tri dans ces informations.
pour la molécule 2 c'est plus simple ,car on identifie 3 fonctions esters .
pour la formule 3, c'est compliqué ,car tu ne l'a pas éditée!.
l'hydrolyse du lactose provoque la cassure de la liaison osidique.Il se forme 2 oses.
l'hydrolyse du triglycéride casse les liaisons esters.
voir cette animation ![]()
l'hydrolyse du peptide casse les liaisons peptidiques et libère les acides aminés


