Inscription / Connexion Nouveau Sujet
Détermination d'un alcène et Composition massique d'un alcène
Bonjour, voilà j'ai besoin d'aide pour deux exercices. j'ai DS demain, et je n'arrive pas à faire ce type d'exercice. est ce que vous pourriez m'expliquer comment faire. Merci 
I-
Un alcène a pour masse molaire M = 56 g/mol. Il est la base de la préparation de MTBE (méthyltertiobuthyléther) utilisé pour améliorer la qualité des supercarburants.
1) a) Écrire la formule générale d'un alcène à n atomes de carbone
b) déterminer sa formule brute
2) L'alcène est ramifié. Donner son nom et sa formule
3) Possède-t-il des stéréo isomères? Justifier la réponse
II- ** exercice effacé et dupliqué dans un nouveau topic ** 
![]() Détermination d'un alcène et Composition massique d'un alcène
Détermination d'un alcène et Composition massique d'un alcène
Edit Coll : merci de respecter la FAQ, un problème = un topic 
![]()
I)
1a) La formule générale des alcènes est CnH2n.
1b) Par conséquent la masse molaire est
M= 12n+2n=14n = 56  n=4. L'alcène a donc pour formule C4H8.
n=4. L'alcène a donc pour formule C4H8.
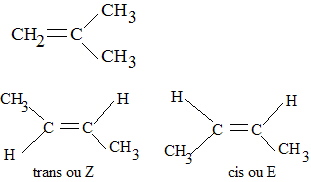
2) Il y a deux isomères a) le but-2-ène b) le 2-méthylprop-1-ène ou méthylpropène (les chiffres n'étant pas nécessaires ici)
seul le méthylpropène est ramifié (voir la première figure).
3) il ne présente de stéréoisomères, mais par contre le but-2-ène présente les isomères E et Z ou Cis et Trans (voir la figure)
II) Deux alcanes ...
1) la formule générale des alcanes est CnH2n+2.
2) pour A, on peut écrire 12n=4,5x(2n+2) n=3, soit C3H8. C'est le propane.
n=3, soit C3H8. C'est le propane.
pour B, vu que la masse molaire vaut M= 12n+2n+2=14n+2, on peut écrire 12n/(14n+2)=80/100 1200n=1120n+160
1200n=1120n+160 n=2. B a donc pour formule C2H6. C'est de l'éthane.
n=2. B a donc pour formule C2H6. C'est de l'éthane.
A votre service
Guytou18
merci beaucoup, j'ai mieux compris, mais je crois que je ne saurais pas le refaire... Encore merci. Bonne soirée


