Inscription / Connexion Nouveau Sujet
Des atomes aux molécules
Bonjour, dans un dm de physique j'ai un exercice sur les atomes et les molécules je ne peux pas recopier l'énoncer car je n'arriverai pas à faire la représentation de Lewis ainsi que le modèle moléculaire d'une molécule. Il est demandé de donner la formule électronique et de déterminer le nombre d'électrons qui marquent sur la couche externe pour qu'elle soit saturé. La je n'ai rencontré aucun problème seulement j'ai 2 questions que je n'arrive pas à dissocier :
1) vérifier que le nombre de doubles non liants dont s'entoure les atomes, autres que celui d'hydrogène, leur permettent de vérifier la règle de l'octet.
2) pour chacun des atomes (1)(2)(3)(4), déterminer le nombre d'atomes liés à l'atome considéré et des doubles non lianes entourant cet atome.
Aux 2 questions je mets :
Carbone : 4 liaisons
Azote : 3 liaisons et 1 doublet non liant
Oxygène : 2 liaisons et 2 doubles non liants
Quelqu'un pourrait me dire ce qui diffère des 2 questions s'il vous plaît ?
Dans la première question, tu vois tout simplement vérifier s'ils respectent la règle de l'octet et dans la seconde, tu dois déterminer le nombre d'atomes liés avec l'atome en question (doublets liants) et également de déterminer les doublets non-liants que comporte l'atome en question
Dans la deuxième question on te demandes que les atomes liés à lui et non leur mode de liaison et après les doublets non-liants. Dans les doublets non-liants on ne parle pas de liaison simple ou double. DOnc non 
Et dans la question suivante on me demande d'utiliser le résultat de la question précédents pour décrire la géométrie de la molécule autour de chacun des atomes, or on la sait grâce au, liaisons simples non ?
En tout cas merci à toi
Bonjour à tous les deux.
Ce serait quand même plus aisé de vous guider si on connaissait le nom et/ou la formule brute du composé étudié.
À plus.
Est tu sûr que tu nous ai donné l'intégralité de la consigne ? Car j'ai l'impression d'avoir eu les questions et non la consigne de départ
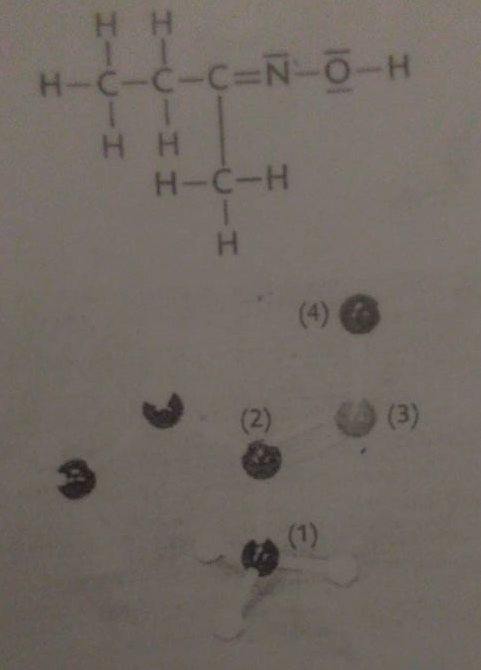
On à un document ou il y à la représentation de la de Lewis de la molécule : méthyléthylcétoxime ainsi que son modèle moléculaire.
1) a)écrire la formule électronique des atomes d'hydrogène (Z=1), de carbone (Z=6), d'azote (Z=7) et d'oxygène (Z=8)
b) déterminer le nombre d'électrons qui manquent sur la couche externe de chaque atome pour qu'il respecte la règle du duet ou de loctet
c) en déduire le nombre de liaisons covalentes que chaque atome peux établir
d) dans la représentation de Lewis proposée, vérifier le nombre de liaisons covalentes établies par chaque atome.
e) vérifier que le nombre de doublets non lianes dont s'entoure les atomes, autres que celui d'hydrogène, leur permettent de vérifier la règle de l'octet.
2) a) pour chacun des atomes (1),(2),(3) et (4) déterminer le nombre d'atomes liés à l'atome considéré et des doublets non liants entourant cet atome
b) utiliser le résultat de la question précédents pour décrire la géométrie de la molécule autour de chacun des atomes
Voici l'intégralité de mon énoncé
En réalité ça change tout, désormais tu dois t'aider de la représentation de Lewis de la molécule. Pour la dernière question, tu dois décrire la situation de chaque atome.
Par exemple : "L'atome de carbone est relié par 2 atomes d'hydrogène par des liaisons simples"... Et ainsi de suite
Donc pour la question 2)a) on doit dire le nombre de liaison simple et de doublet non liant pour ensuite trouver la géométrie de la molécule ?
La représentation de Lewis dont vous disposez doit ressembler à quelque chose comme cela...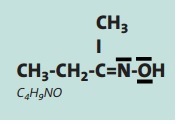
La première question est une application directe du cours de seconde.
Pour la seconde, il faudrait savoir à quels atomes se rapportent les n° (1),(2),(3) et (4).
Qu'est-ce qui vous arrête pour le 2-a ?
Il suffit de compter sur la photo du modèle moléculaire.
Je vous donne un exemple, celui du carbone (1).
Il s'agit d'un atome C, qui forme 4 liaisons covalentes simples...
3 avec des atomes H
1 avec un autre atome C (celui qui est noté (2)).
Et pour répondre à la question 2-b...
L'atome (1), lié à 4 autres atomes par des liaisons simples, a donc une structure tétraédrique.
A vous la suite.
J'ai mis pour la (1) : 4 atomes liés à l'atome considéré, 0 doublet non liant et 4 liaisons simples donc tetraedrique c'est pareil ?
J'ai réussis seulement pour la (3) j'ai pas trouve de géométrie avec une liaison simple et une double
J'ai mis pour la (1) : 4 atomes liés à l'atome considéré, 0 doublet non liant et 4 liaisons simples donc tetraedrique c'est pareil ?
J'ai réussi seulement pour la (3) j'ai pas trouvé de géométrie avec une liaison simple et une double
Autour de l'atome d'azote noté (3), la molécule est donc coudée.
Pensez à noter que cet atome, qui forme 1 liaison double (càd 2 doublets liants), 1 liaison simple (1 doublet liant) et qui porte 1 doublet non liant, est donc entouré par 2 + 1 + 1 = 4 doublets soient 4
 2 = 8 électrons ; la règle de l'octet est donc satisfaite pour cet atome.
2 = 8 électrons ; la règle de l'octet est donc satisfaite pour cet atome.
Qu'est-ce qui vous arrête pour les atomes (2) et (4) ?
P.S. Je ne connais pas très bien le contenu du programme actuellement enseigné en 1°S, avez vous entendu parler de la méthode VSEPR ?
D'accord merci par contre je dois le noté ou le truc ou il est écrit 8 électrons ?
Pour le (2) j'ai mis 2 liaisons simples, 1 liaison double : plane triangulaire et le (4) : 2 liaisons simples, 2 doublets non lianes : plane coudee
D'accord merci par contre je dois le noté ou le truc ou il est écrit 8 électrons ?
En fait, je crois que vous l'avez déjà fait en répondant aux questions 1-d et 1-e.
Pour le (2) j'ai mis 2 liaisons simples, 1 liaison double : plane triangulaire et le (4) : 2 liaisons simples, 2 doublets non lianes liants : plane coudee

Je résumé toutes mes réponses :
1)a) Hydrogène : (K)1
Carbone : (K)2(L)4
Azote : (K)2(L)6
b) hydrogène : 1 électron
Carbone : 4
Azote : 3
Oxygène : 2
c) hydrogène : 1 liaison covalente
carbone : 4
Azote : 3
Oxygène : 2
d) j'ai mis pareil que c)
e) carbone : 0 doublets non liants
Azote : 1
Oxygène : 2
On remarqué le nombre de doublets non liants sont s'entoure les atomes permet bien de vérifier la règle de l'octet.
2) je vois l'avez déjà envoyé et du coup le (3) j'ai mis molécule plane coudée
Au fait, je viens de relire une de vos précédentes réponses...
Pour le (2) j'ai mis 2 liaisons simples, 1 liaison double : plane triangulaire
Azote : (K)2(L)6
(K)2 (L)5
Sauf erreur de ma part, je crois que tout est OK.