Inscription / Connexion Nouveau Sujet
Couples redox
Bonjour j'ai une question
Si on introduit le cuivre dans une solution d'acide nitrique, quelle réaction va se produire prioritairement ?
Couples redox en présence H3O+/H2
Fe2+/Fe
NO3-/NO
Sachant que l'ion hydronium et l'ion nitrate sont tous deux plus oxydant que l'ion Fer II
Merci de m'aider
Bonsoir
La réaction prédominante se produit entre l'oxydant le plus fort d'un couple et le réducteur le plus fort d'un autre couple. Classe les couples en fonction du pouvoir oxydant de l'oxydant du couple et tu pourras répondre.
Cependant ton énoncé est incomplet et incohérent : j'imagine qu'on introduit du cuivre dans une solution d'acide nitrique. Il faut donc des renseignements sur le couple Cu2+/Cu ; le fer n'intervient pas ici. Si tu pouvais fournir un énoncé complet...
Ah je m'excuse, on introduit le fer et dans ce cas le fer et l'ion nitrate réagiront preferentiellement ensemble ?
Ton énoncé est incomplet : pour répondre avec précision, il faut être capable de classer les trois couples. Ton énoncé ne précise pas si l'ion nitrate est un oxydant plus ou moins fort que l'ion oxonium. Il serait aussi intéressant d'introduire dans le classement le couple Fe3+/Fe2+. Tous les livres de première fournissent ce genre de données.
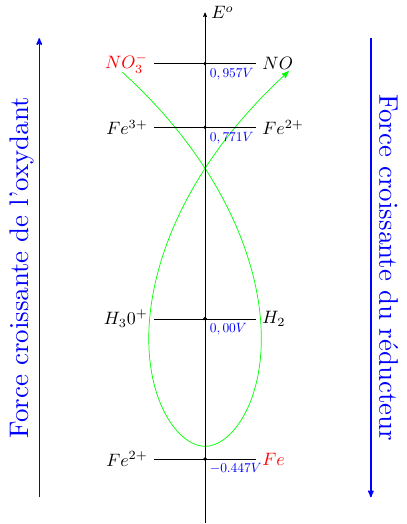
Pour t'aider un peu, voici une classification des divers couples susceptibles d'intervenir ici. Cela ne semble pas demandé par l'énoncé mais il serait intéressant d'étudier successivement les deux cas :
1° : introduction d'un peu de fer dans une solution diluée d'acide nitrique ;
2° : introduction d'un peu de fer dans une solution d'acide chlorhydrique.
PS : l'action de l'acide nitrique concentrée n'est sûrement pas à ton programme.