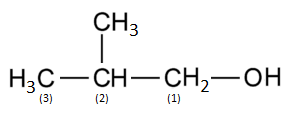Inscription / Connexion Nouveau Sujet
Composé organique oxygéné
Bonjour,
L'exercice ci-dessous me pose quelques difficultés. Pouvez-vous corriger mes réponses et m'aider à répondre aux questions 3 et 4. Merci.
Un composé organique oxygéné a pour formule brutevC4H10O. Son oxydation ménagée par les ions dichromate en milieu acide conduit à un produit donnant des tests positifs avec la DNPH et le réactif de Schiff et de formule C4H8O
1.Sachant que la molécule de ce composé est ramifiée , donnez sa fonction, sa formule semi-développée et son nom.
2. Ecrivez la réaction d'oxydo-réduction entre ce composé et les ions dichromate sachant que ces derniers sont réduits en ions chrome Cr3+.
3. Calculez la masse de composé oxydé, si l'oxydation a nécessité 200 ml de solution oxydante à 0,50 mol.l-1.
4. Ľexpérience montre qu'avec 200 ml supplémentaire de solution oxydante, l'oxydation se poursuit et conduit à un autre composé. En isolant ce composé par une distillation, on ajoute au distillat quelques gouttes mde BBT qui vire au jaune.
Justifiez cette observation et écrivez l'équation dďoxydo-réduction correspondante.
Données:
M(H)=1 g.mol-1
M(C)= 12g.mol-1
M(O)= 16 g.mol-1
Réponses
1. CH3-C(O)-CH2-CH3
Cétone: Butan-2-one
2.
3.
4.
Bonjour,
Ta réponse à la question 1) ne peut pas être exacte car :
a) Les cétones ne réagissent pas avec le réactif de Schiff.
b) L'énoncé précise que la molécule cherchée est ramifiée.
Effectivement le réactif de Schiff permet de déceler le présence ďun aldéhyde et de le distinguer des cétones. Je pensais que c'était la cétone car le test est positif en DNPH, mais cela ne suffit pas. Erreur de ma part.
C'est donc un aldéhyde:
CH3-CH(CH3)-C(H)=0
2-méthylpropane
Et j'oubliais ce que j'aurais du mettre en premier :
D'après l'énoncé la formule brute de la molécule cherchée est C4H10O ce qui n'est pas le cas de celle que tu proposes.
Je n'arrive pas à trouver une molécule qui a une formule brute C4H10O et est ramifiée. J'ai essayé toutes les combinaisons possibles. Je trouve C5H10O.
La molécule que tu cherches n'est pas un aldéhyde.
Il faut lire l'énoncé attentivement.
Celui ci indique que la molécule cherchée donne par oxydation ménagée un produit en qui on peut reconnaître un aldéhyde.
Mais l'énoncé ne dit pas que c'est la molécule cherchée elle même en qui on peut reconnaître un aldéhyde.
Je m'embrouille depuis que j'ai vu un shéma sur l'oxydation ménagée de l'alcool I, qui aboutit à l'aldéhyde puis l'acide carboxylique.
Je trouve pour la 1.
Alcool primaire
3-méthylpropan-1-ol
CH3-CH2(CH3)-CH2-OH
2 méthylpropan-1-ol
Pendant qu'on y est, je ne sais pas dans quel sens mettre l'indice en bas des molecules. De gauche à droite ou le contraire ??
2 méthylpropan-1-ol
Plus exactement :
2 - méthylpropan -1- ol
Pendant qu'on y est, je ne sais pas dans quel sens mettre l'indice en bas des molecules. De gauche à droite ou le contraire ??
L'atome de carbone qui porte le groupement -OH doit avoir le plus petit numéro.
Merci.
La 2 est-elle correct ?
2. Ecrivez la réaction d'oxydo-réduction entre ce composé et les ions dichromate
2.
Oui, cette demi-équation est exacte, mais elle n'est qu'une partie du travail demandé.
Il faut y ajouter l'autre demi-équation et enfin à partir de ces deux demi-équations répondre à la question posée.
L'autre demi-équation:
R-CH2-OH=R-CHO+2H++2e-
Equation-bilan:
Pour la 3. comment faire ?
3. Calculez la masse de composé oxydé, si l'oxydation a nécessité 200 ml de solution oxydante à 0,50 mol.l-1.
Tes équations sont correctes.
Toutefois tu as14H+ dans les réactifs et 6H+ dans les produits.
On élimine les espèces qui interviennent de manière équivalente.
On retire donc 6H+ des réactifs et 6 H+ aussi dans les produits
On obtient :
Question 3 :
a) Tu calcules la quantité de matière nox de solution oxydante utilisée.
b) Tu te sers de l'équation de la réaction pour en déduire la quantité de matière nred d'alcool oxydé.
c) A partir de la quantité de matière nred et de la masse molaire tu réponds à la question posée.
nox=CV=0,50×0,2=0,1mol
OK
Je ne vois pas ce que je dois faire pour la b)
Les quantités de matière nox et nred ayant réagi sont proportionnelles aux coefficients stchiométriques de l'équation chimique.
Comme tu peux le constater par toi même ces coefficients sont " 1 " pour l'oxydant (Cr2O7)2- et " 3 " pour le réducteur RCH2OH
Non.
Comment as tu obtenu ce résultat ?
Merci de toujours accompagner un résultat par le calcul qui va avec, cela me permet de situer les raisons d'une éventuelle erreur ( comme c'est le cas ici )
J'ai additionner tous les coefficiants stochiométrique, puis j'ai muplitiplie celui-ci par nox. Je ne sais pas pourquoi j'ai fait ça. C'est passé par ma tête quand vous m'avez dit que "nox et nred ayant réagi sont proportionnelles aux coefficients stchiométriques de l'équation chimique."
À vrai dire, je n'ai toujours pas compris pour la b). Pouvez-vous me réexpliquer s'il vous plaît. Merci
Il faudrait tout de même savoir ce qu'est la proportionnalité !!!
On dit que deux nombres " a " et " b " sont proportionnels à deux autre nombres " c " et " d " si (a/c) = (b/d) ou ce qui revient au même si (a/b) = (c/d) ou bien encore si a*d = b*c
Donc dire que nox et nred sont proportionnels à 1 et 3 revient à dire que nox / 1 = nred / 3
nred=30mol
c) A partir de la quantité de matière nred et de la masse molaire tu réponds à la question posée.
m=n.M=30×75=2250g
nred=30mol
Non.
Comment as tu obtenu ce résultat ?
Merci de toujours accompagner un résultat par le calcul qui va avec, cela me permet de situer les raisons d'une éventuelle erreur ( comme c'est le cas ici )
OK pour nred = 0,3 mol
En revanche je trouve que M(C4H10O) = (4*12)+(10*1)+(1*16) = 74 g/mol
et que :
m((C4H10O)) = 0,3 * 74 = 22,2g
Oui, c'est bien ça
Je rectifie mon erreur, ce n'est pas 75g.mol
4. Ľexpérience montre qu'avec 200 ml supplémentaire de solution oxydante, l'oxydation se poursuit et conduit à un autre composé. En isolant ce composé par une distillation, on ajoute au distillat quelques gouttes mde BBT qui vire au jaune.
Justifiez cette observation et écrivez l'équation dďoxydo-réduction correspondante.
On sait que le composé organique oxygéné est un alcool primaire. Il subit une oxydation ménagé. Celui-ci devient alors un aldéhyde. L'oxydation se poursuit et conduit à un acide carboxilique.
En utilisant du BBT dans une solution acide verra la couleur passer au jaune.
L'équation n'est-elle pas la même ?
Oui, tout se passe comme tu l'a indiqué.
La réaction d'oxydo réduction n'est pas exactement la même, mais elle lui ressemble beaucoup.
La différence essentielle provient de la demi réaction décrivant la transformation de l'aldéhyde R-CHO en acide carboxylique R-COOH