Inscription / Connexion Nouveau Sujet
Classification perriodique
bonjour
voici mon exercice:
Compléter le ta bleau suivant en utilisant la classification périodique
| Symbole | K | Be | Cl | P |
| Nom | Potassium | Bérylium | Chlore | Phosphore |
| Numéro atomique | 19 | 4 | 17 | 15 |
| Structure électronique | (K)2(L)8(M)8(N)1 | (K)2(L)2 | (K)2(L)8(M)7 | (K)2(L)8(M)5 |
| Ion stable formé | ||||
| Structure électronique de l'ion |
ce qui est souligner, est ce qui est déjà marquer dans le tableau et ce qui est en italique sont mes réponses.Mais je ne sais pas ce que c'est un ion stable pouvez-vous m'aider à remplier les 2 dernière lignes.
merci d'avance
Bonjour,
Un ion est stable si :
-pour Z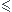 4, il a 2 électrons dans sa dernière couche (K ou L), c'est la règle du duet
4, il a 2 électrons dans sa dernière couche (K ou L), c'est la règle du duet
-pour Z 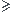 5, il a 8 électrons dans sa dernière couche (L, M, N ...), c'est la règle de l'octet
5, il a 8 électrons dans sa dernière couche (L, M, N ...), c'est la règle de l'octet
Donc pour le potassium K, il perd un électron pour devenir K+ (avec 19 protons et 18 électrons) et avoir 8 électrons dans sa dernière couche (M), respectée la règle de l'octet.
Le béryllium est déjà stable mais tu peux aussi former un ion Be2+ (couche (K)2 saturée)
Pour le chlore, il manque un électron pour respecter la règle de l'octet, il devient Cl-
(K)2 (L)8 (M)8
Pour le phosphore, il manque 8-5 = 3 électrons
Voilà sauf erreur, as-tu compris ?
cela fait:
Symbole K // Be // Cl // P
Nom Potassium // Bérylium // Chlore // Phosphore
Numéro atomique 19 // 4 // 17 // 15
Structure électronique (K)2(L)8(M)8(N)1 //(K)2(L)2 //(K)2(L)8(M)7 //(K)2(L)8(M)5
Ion stable formé octet // duet // octet //octet
Structure électronique de l'ion K+ // Be2+ //Cl- //P3+
non 
Pour l'ion stable, c'est la formule de l'ion qu'on te demande donc K+, Be ou Be2+, Cl-
et P3- car P gagne 3 électrons : 3 charges négatives et pas positives!!!
P3+ ne serait pas stable et n'existe pas : (K)2 (L)8 (M)2 la règle de l'octet n'est pas respectée puisque (M) n' a que 2 électrons au lieu de 8 !
Pour les structures, c'est comme avnt sauf que tu rajoutes ou enlèves les électrons pour que l'ion soit stable
Pour K+ (K)2 (L)8 (M)8
Pour Be2+ (K)2 (L)4 ou (K)2
Pour Cl- (K)2 (L)8 (M)8
Pour P3- (K)2 (L)8 (M)8


