Inscription / Connexion Nouveau Sujet
Chimie
Bonsoir, je ne trouve pas la formule semi dvp de cette molécule :/
Bonjour Krayz : ( je ne peux pas dessiner la structure avec mon "Mac" )
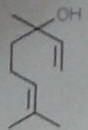
Il s'agi de la molécule du linalol C10H18O .
Nom chimique 3,7-diméthyl-1,6-octadién-3-ol .
CH2=CH-C[(CH3)(OH)]-CH2-CH2-CH=C(CH3)2 . ( le carbone 3 est porteur du CH3- et du -OH ) .
Bonnes salutations .
Merci 
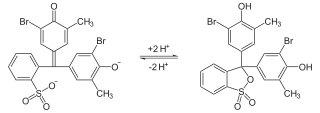
Une petite question : concernant cet indicateur colorée le pourpre de bromocresol , pouvez vous m'indiquer le nombre de doubles liaisons conjuguées s'il vous plaît des deux formes![]()
Je n'arrive pas à joindre en pièce jointe je suis sur mon tel
11 doubles liaisons conjuguées et 4 je trouve quen pensez vous
***Lien url ajouté***
Dernière question pour ce thème svp : comment déterminer la géométrie de cette molécule autour des atomes principaux svp
CH4S
Pose en autant que tu veux:
Par contre, je peux savoir qu'elles sont les atomes principals ?
Sache que les liaison (liant ou non lian) ce repousse au maximum
Ok,
Donc tu as a peux pres :
H
|
H------C-------S------H
|
H
Pour determiner la geometrie, il te faut d'abord determiner la formule de Lewis, Ok ?
La geometrie autour de l'atome C est tetraedrique: en effet, c'est le centre d'un tetraedre. Car les 4 liaison ce repousse au maximum (je vais mettre l'image pour que tu puisse voir..)
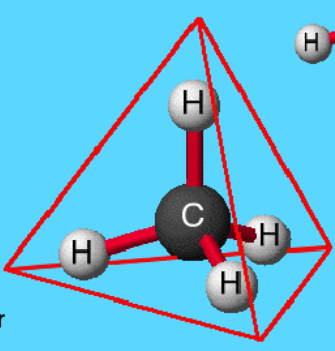
Pour le soufre, son mumero atomique est 16, sa structure electr est donc (K)2(L)8(K)6, il forme donc 2 liaison ( une avec le carbone et une avec l'hydrogene) et forme 2 doublet non liant OK ? (Car il lui reste 4electrons de valence..).
Tu as donc
-
....................S---H
-
N'est ce pas ? La structure est donc coudé car les liaison se repousse tous, c'est pareil pour la molecule d'eau H2O que je vais te joindre
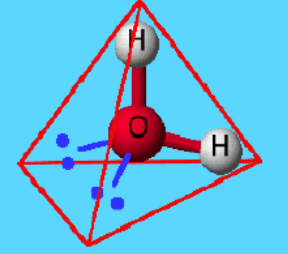
Je te prend l'exemple de l'eau car c'est la seul que je trouve sur internet pour te l'illustrer.
Considere ici l'oxygene pour le soufre, et les 2 hydrogene pour un carbone et un hydrogene, ok ? Donc du fait qu'il se repoussent, ca fait l'image d'un "coude".
La geometrie est donc coudé.
Eh bien, tu ne peux pas donner une geometrie commune..
La geometrie autour du Carbone est tetra et celle autour du soufre est coudé, dans un exercice avec une molecule tel, on te demandera de determiner la geometrie autour d'un atome en particulier
Donc la réponse est : Trétraédrique pour les atomes autour de C et coudée pour ceux autour de S ?
la réponse convient ?