Inscription / Connexion Nouveau Sujet
Avancement d'une réaction chimique
Bonjour à tous,
J'aurai besoin d'aide pour cet exercice svp
Je bloque pour la question 3 car je n'est pas trop compris cette histoire de mélange stoechiométrique
J'ai essayé de faire le tableau
En présence d'ions hydroxyde HO- , les ions fer II Fe2+ réagissent pour former un précipité vert d'hydroxyde de fer Fe(OH)2
Les ions fer II constituent le réactif limitant et leur quantité initiale est de 5,0 mmol
1. Etablir le tableau d'avancement du système étudié
2. Déterminer la valeur de l'avancement maximal Xmax
3. Calculer la quantité initiale des ions hydroxyde qui correspondrait au mélange stoechiométrique.
Merci d'avance
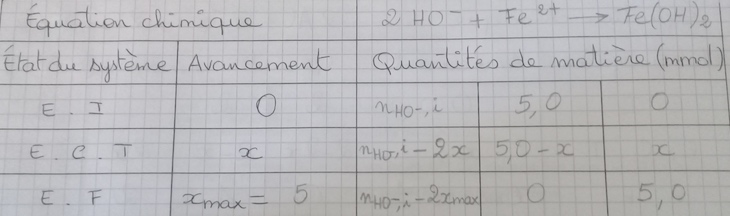
Salut,
Mélange stoechiométrique => ni(Fe2+) = ni(HO-)/2 (tu établis l'égalité en divisant les quantités de matière initiales par leur coefficient stoechiométrique).
Tu as l'avancement maximal, donc le réactif limitant. En utilisant le tableau, tu as ... ?

Oui !
C'est d'ailleurs ce que tu peux retrouver avec ton tableau à l'état maximal :
ni(HO-) - 2xmax = 0
<=> ni(HO-) = 2xmax
or d'après l'énoncé, xmax = 5mmol
donc ni(HO-) = 10 mmol

Bonjour comment as-tu fait pour calculer l'avancement maximal comme pour HO- il n'y a pas de valeur de quantité initiale stp ?


