Inscription / Connexion Nouveau Sujet
acide et base question cours
 Bonjour, j'ai une question concernant la définition d'une réaction acido-basique.
Bonjour, j'ai une question concernant la définition d'une réaction acido-basique.
"Une réaction acido-basique est une réaction qui implique un transfert de un ou plusieurs protons entre les réactifs". Je vois pas comment les protons peuvent être transférer (appart avec des réaction nucléaire car le noyau est hyper solide) pourtant c'est que les électrons qui sont modifiés !  Merci..
Merci..
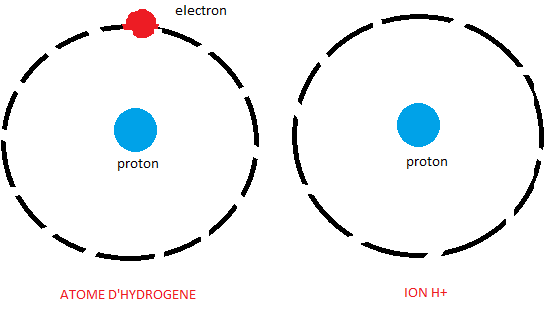
c'est surtout qu'on utilise le mot proton pour faire savant mais on ferait mieux de dire un ion H+, ça passerait mieux ^^
effectivement ça ne sont pas des réactions nucléaires mais des réactions chimiques donc qui n'influe pas sur le noyau ! (les éléments chimiques sont conservés). En fait dans une réaction acido-basique, il y a simplement des ions H+ qui se détachent de certaines molécules pour aller s'accrocher à d'autres
et c'est plutôt H30+/H2O plutot que H20/H3O+..
Voilà je me demande toujour si HO- est un ampholte vu les couples acide/basique que j'ai fait plus haut à 1h14.
Pareil pour l'ammoniac :
NH4+/NH3
NH3/NH2-

je ne crois pas que le couple HO-/O2- existe
H2O est ampholyte mais pour HO- je ne crois pas
l'ammoniac est en effet un ampholyte
Ouai.. pourtant y'a bien transfert d'ion H+ et les 2 ions existent (ion hydrogène et ion oxygène), quelqu'un d'autre peut p'tete nous aider!