Inscription / Connexion Nouveau Sujet
1ere S chimie: concentrations
Bonjour!
voila l'énoncé de l'exo que j'arrive pas à faire:
L'eau de Javel est obtenue par babotage du gaz dichlore Cl2 dans une slution d'hydroxyde de sodium.
Elle contient des ions sodium Na+(aq) , chlorure Cl-(aq) , et hypochlorite ClO-(aq) qui donne a l'eau de javel ses propriétés spécifiques.
L'eau de javel commercale, vendue en berlingots de 250mL, a une concentration molaire en ions hypochlorite de 2 mol/L. Cela correspond à "48°chl" (degrés chlorométriques).
a) Quelle est la concentration molaire en ions hypochlorite de l'eau de javel obtenue en complétant avec de l'eau le cotenu du berlingot versé dans un flacon d'un litre?
b) Le degré chlorométrique d'une eau de Javel est défini comme étant égal au volume de dichlore (en L) utilisé pour préparer un litre de cette eau de javel, selon la réaction d'équation:
Cl2(g) + 2HO-(aq)  ClO-(aq) + Cl-(aq) + H2O(l)
ClO-(aq) + Cl-(aq) + H2O(l)
Montrer qu'une eau de javel dont la concentration molaire en ions hypochlorite est 2 mol/L correspond bien a 48°chl (on prendra Vm=24L/mol) .
On construira pour cela le tableau d'avancement de la réaction, en utilisant le fait que l'on connait ici l'état final du système.
Voila mon exo j'arrive vraiment pas à le faire mm si j'ai bossé dessus...
Merci de m'aider!
Bonsoir,
Si c'était urgent, il aurait fallu le poster au début des vacances et pas au dernier moment!
1) On applique CV=C'V' => C'=CV/V'=2*0,250/1= 0,5 mol/L
2)D'après l'équation 1 mol de Cl2 produit 1 mol d'ions hypoclorite.
Donc pour avoir 2 mol/L d'ions hypochlorite, il fallait avoir au départ 2 mol de Cl2 qui occupent donc 2*24 = 48 L
Cl2 + 2OH- ---> ClO- + Cl- + H2O
Initial 2 y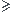 4 ---> 0 0 0
4 ---> 0 0 0
Avancement 2-x y-2x ---> x x x
Final 0 y-4 ---> 2 2 2
A+


