Inscription / Connexion Nouveau Sujet
Pka d'un couple acide/base; équilibre chimique; pH
Bonjour à tous, j'ai un peu de mal avec cet exercice pouvez-vous m'aider à le resoudre :
Voici l'énoncé
On considere deux couples acide/base :
-couple (I) : acide acétylsalicylique C8H7O2CO2H/ ion acétylsalicylate C8H7O2CO2-
-couple (II): acide acétique CH3CO2H/ ion acétate CH3CO2-
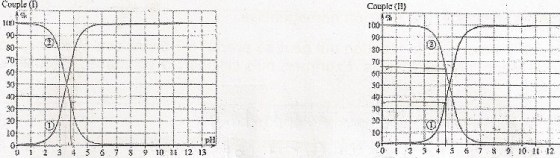
Les diagramme de distribution relatives à ces deux couples sont données ci dessous. Ils donnent l'évolution des pourcentages en acide et en base conjuguée en fonction du PH .
Voici mes pistes de reflexions et les questions :
1) Déterminer à l'aide des diagrammes de distribution, les pKa des deux couples (pka1 relatif à l'acide acétylsalicylique et pka2 relatif à l'acide acétique
Alors je trouve pka1= 3.5 et pka2= 4.8
I) Etude des espèces seules
2) On prepare une solution S en mélangeant V1= 10 ml de solution d'acide acétylsalicylique de concentration C= 1.10^-2 mol/L et V2=20 ml de solution d'acétylsalicylate sodium, Na+ + C8H7O2CO2- , de meme concentration. On homogenise et on mesure le PH. On obtient : pHs= 3.8 .Determiner la valeur du quotient [C8H7O2CO2-]s/ [C8H7O2CO2H]s
Alors je trouve comme valeur 9.8 10^-5
3) On prepare une solution S' en mélangeant V'1= 10 ml de solution d'acide acétique de concentration C= 1.10^-2 mol/L et V2=20 ml de solution d'acétate de sodium, Na+ + CH3CO2- , de meme concentration. On homogenise et on mesure le PH. On obtient : pHs'= 4.5 .Determiner la valeur du quotient [CH3CO2-]s/ [CH3CO2H]s
Alors Je trouve comme valeur 1.85
II) Etude du mélange
4) On mélange les solutions S et S' et on homogénise.
Quelle est la nature de la reaction qui peut se produire ? Ecrire son équation, l'acide acétique etant l'un des réactifs. Exprimer, puis calculer, la constante d'équilibre K qui lui est associée.
Je trouve CH3CO2H + C8H7O2CO2- = CH3CO2- + C8H7CO2H et
K= 1.88 10^4
A partir de là, je n'arrive plus à poursuivre le probleme. Pouvez vous m'aider svp.
5) Expliquer pourquoi avant toute reaction, les quotients calculus précédemment ne sont pas modifies par le mélange de S et S'.
6) Le PH du mélange S + S' obtenu vaut : PHs+s'= 4.15
Déterminer la valeur des quotients : [C8H7O2CO2-]s+s'/ [C8H7O2CO2H]s+s' et [CH3CO2-]s+s'/ [CH3CO2H]s+s'
7) Dans quel sens le systeme S+S' a-t-il évolué? Cette évolution était-elle prévisible ? Justifier la reponse.
III) En utilisant les memes solutions qu'en I) , on prepare :
- Un mélange S avec V1= 1 ml et V2= 10 ml
- Un mélange S' avec V'1 = 10 ml et V'2= 1 ml
On mélange S et S' : soit S+ S' le système obtenu.
8) Prevoir l'évolution de ce système
9) Etablir un tableau d'avancement et exprimer le quotient de reaction associé à l'équation en fonction de l'avancement x de la reaction.
10) Vérifier qu'à l'équilibre final, xeq= 1.01 mol. Quelle valeur peut-on avoir pour PHs+s' ?
L'image des diagramme est attachée ci-dessous.
Voila, pouvez vous m'aider svp et me dire si mes reponses sont justes. Merci d'avance.