Inscription / Connexion Nouveau Sujet
Modulation/Demodulation DBSP et DBAP
l'avantage de la modulation "DBAP" c'est la simplicité de l'opération de la démodulation notamment une simple détection d'enveloppe suffirait mais je me demande pourquoi ne pas faire de même pour la "DBSP" puisque l'existence d'un enveloppe est aussi remarquable : c a d pour quoi ne pas démoduler un signale "DBSP" avec une détection d'enveloppe ?
Bonjour,
La modulation "Double Bande Avec Porteuse" peut être démodulée par détection d'enveloppe parce que l'amplitude de l'onde est identique au signal modulant. Il suffit donc de "redresser" le signal et de filtrer pour récupérer le signal modulant.
La modulation "Double Bande Sans Porteuse" ne peut pas être démodulée par détection d'enveloppe parce que l'amplitude de l'onde n'est pas identique au signal modulant. Il y a effectivement une enveloppe (remarquable ou pas ) dont la détection d'enveloppe ne restitue pas le signal modulant.
) dont la détection d'enveloppe ne restitue pas le signal modulant.
Bonjour,
Merci pour votre réponse .
Je suis d'accord avec vous que l'amplitude va être "modifiée" mais dans la transmission d'un signal l atténuation avec un facteur 1/2 de l'amplitude ne forme pas "grave" modification et donc c'est négligeable ( à savoir une amplification fera l'affaire ) n'est ce pas ??
Toujours D'accord avec vous : Dans la modulation DBSP (Double Bande Sans Porteuse) Ce qui est remarquable notamment ce n'est pas l'existence d'enveloppe certes , mais c'est la conformité de cet enveloppe avec le signale modulant .
(Désolée de vous déranger mais Marc, si tu as le temps pourrais tu passer sur cet exo? https://www.ilephysique.net/sujet-dosage-243133.html Cette fois je n'y arrive pas trop... Merci. Bon travail)
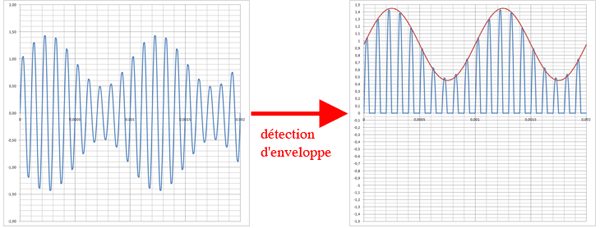
Premier schéma : une modulation DBAP et une détection d'enveloppe. Un filtrage donne la courbe en rouge qui est le signal modulant. Donc, dans ce cas, une détection d'enveloppe et un filtrage permettent de retrouver le signal modulant (à une composante continue près).
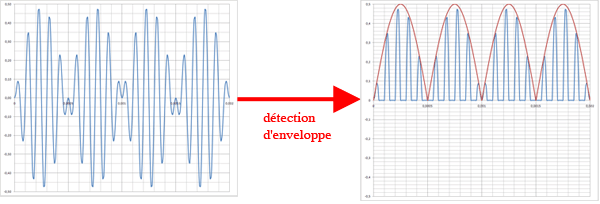
Deuxième schéma : une modulation DBSP et une détection d'enveloppe. Un filtrage donne la courbe en rouge. Donc, dans ce cas, une détection d'enveloppe et un filtrage donnent la valeur absolue du signal modulant donc on ne retrouve pas le signal modulant par une détection d'enveloppe.
Oui en effet mais avec lui je comprends moins bien (par exemple dans réponse il introduit des grandeurs pas définies dans l'énoncé et je comprends moins facilement.. tu vas me dire "ben c'est pas si dur de comprendre ce qu'il dit", mais bon)
Je ne l'aurais pas forcément expliqué comme ça, notamment pour le choix de l'équation de H2O2...
Je veux bien te répondre mais je vais faire ce que je n'aime pas que les autres font c'est-à-dire intervenir alors que la discussion est lancée.
Apparemment, il n'y a pas de réponse de taktouk2010, le créateur de ce topic. Tu me diras que ce n'est pas mieux de pirater un autre topic et de le détourner.
Je vais faire l'exo (TP ? ) en entier parce que je n'ai pas fini et je pourrais mettre des réponses.
Ta courbe n'a pas l'air exceptionnelle mais, bon, on fera avec...
"je vais faire ce que je n'aime pas que les autres font" ==< En bon français, c'est peut-être "je vais faire ce que je n'aime pas que les autres fassent "
Pour la question 1
L'équation de dissolution du sel de Mohr :
Fe(NH4)2(SO4)2,6H20 --> Fe2+ + 2 NH4+ + 2 SO42- + 6 H2O
On a 100 mg/L de Fe2+. Donc on a 0,1 / 56 = 1,8.10-3 mol/L de Fe2+.
D'après l'équation, on a le même nombre de moles de sel de Mohr (masse molaire = 392 g).
Donc (0,1 / 56) 392 = 700 mg de sel de Mohr par litre d'eau.
Le protocole, tu dois savoir aussi bien que moi. En gros, on met à peu près la moitié de l'eau nécessaire dans un bécher. On pèse le sel de Mohr (en considérant qu'il est pur). On verse le sel de Mohr dans l'eau et on rince le récipient qui contenait le sel de Mohr en récupérant l'eau dans le bécher. On peut utiliser un agitateur magnétique pour faciliter la dissolution.
On complète jusqu'au trait de jauge indiquant 1 litre. On n'est d'ailleurs pas obligé de faire un litre mais il faut ajuster la quantité de sel de Mohr en conséquence.
Cela te convient ?
Pour la 2
Tu as la réponse... Effectivement, 20 mL de solution mère dans un bécher de 100 mL et on complète avec de l'eau distillée. On obtient une solution à 20 mg/L parce que :
C1V1 = C2V2
on part de la solution mère C1 = 100 mg/L dont on prend V1 pour obtenir C2 = 20 mg/L avec un volume de V2 = 100 mL (par exemple).
100 x V1 = 20 x 100
V1 = 20 mL
Pour la 3
Il faut savoir si Fe2+ est un réducteur ou un oxydant. L'eau oxygénée peut être réducteur ou oxydant selon qu'elle se trouve avec un réducteur ou un oxydant (d'où les deux équations que tu donnes).
Dans le texte, on dit :
on oxyde les ions Fe2+ à l'aide de l'eau oxygénée H2O2 en milieu acide
On ne peut oxyder qu'un réducteur. Effectivement, dans les réactions d'oxydo-réduction, le réducteur est oxydé et l'oxydant est réduit. Donc Fe2+ est un réducteur d'après l'énoncé. Si ça ne nous suffit pas, il faut se rappeler qu'un réducteur donne des électrons. Si Fe2+ est transformé en Fe3+, Fe2+ est obligé de céder un électron : Fe2+ = Fe3+ + e- (pour satisfaire l'équilibre électrique). Donc Fe2+ cède des électrons, c'est donc un réducteur.
Donc H2O2 est un oxydant. Un oxydant capte des électrons (cédés par le réducteur).
H2O2 + 2 H+ + 2 e- = 2 H2O
Les ions H+ parce que c'est en milieu acide.
Donc l'équation totale est :
2 Fe2+ + H2O2 + 2 H+ = 2 Fe3+ + 2 H2O
Holala encore une avalanche de détails ! (ce qui est super!)  La question 1) me semble tout à fait parfaite, je regarde le reste, j'essaie de comprendre
La question 1) me semble tout à fait parfaite, je regarde le reste, j'essaie de comprendre 
merci Marc
Je reviens demain te poser une ou deux questions sur ce que tu as écrit et aussi sur les questions qui suivent 
Pour la question 1)
D'après l'équation, on a le même nombre de moles de sel de Mohr (masse molaire = 392 g).
Donc (0,1 / 56) 392 = 700 mg de sel de Mohr par litre d'eau.
C'est 392 g/mol je crois. Sinon, on a le même nombre de moles de sel de Mohr entre où et où? Je n'ai pas bien compris ça
 Et, quand tu parles de nombre de moles, tu parles de quantité de matière c'est bien ça?
Et, quand tu parles de nombre de moles, tu parles de quantité de matière c'est bien ça? 
Est ce qu'une fiole jaugée de 1L existe? Donc en fait, on remplit un bécher (de 1L aussi?
 ) à moitié, on pèse 700g de sel de Mohr, on les verse dans ce bécher. On met le contenu du bécher dans une fiole jaugée de 1L et on remplit avec de l'eau distillée jusqu'au trait de jauge sans qu'il reste du sel dans le bécher. Si j'ai bien compris.
) à moitié, on pèse 700g de sel de Mohr, on les verse dans ce bécher. On met le contenu du bécher dans une fiole jaugée de 1L et on remplit avec de l'eau distillée jusqu'au trait de jauge sans qu'il reste du sel dans le bécher. Si j'ai bien compris.
Pour la question 2)
Ok. C'est clair

Pour la question 3)
J'ai compris comment résoudre le dilemme

Pour la question 4)
On peut pas se servir de l'équation de la question 3) déjà car on a pas l'acide chlorhydrique dedans. Je ne capte pas ce concept de "suffisant", suffisant pour que quoi?
Fe(NH4)2(SO4)2,6 H20 --> Fe2+ + 2 NH4+ + 2 SO42- + 6 H2O
S'il y a n moles de Fe(NH4)2(SO4)2,6 H20 , d'après l'équation, il y a :
n moles de Fe2+
2n moles de NH4+
2n moles de SO42-
C'est la raison pour laquelle j'ai écrit :
D'après l'équation, on a le même nombre de moles de sel de Mohr
sous-entendu ==> le même nombre de moles que Fe2+.
La masse molaire du sel de Mohr est 392 g/mol effectivement. Mais, si j'écris vite, si je dis "la masse molaire est 392 g", l'information est suffisante. Si j'écris "la masse molaire est 392 g/mol", l'information est redondante. Mais ce n'est qu'un détail...
Et, quand tu parles de nombre de moles, tu parles de quantité de matière c'est bien ça?
Oui.
Est ce qu'une fiole jaugée de 1L existe?
Je ne suis pas assez pointu en chimie pour te l'assurer mais tu peux prendre 500 mL et 350 g de sel de Mohr.
Si j'ai bien compris
Tu as bien compris
Pour la question 4, "suffisant" veut dire qu'il y en a assez pour que la réaction se produise. Autrement dit, il y a un nombre de moles supérieur ou égal au nombre de moles nécessaire. Il peut y avoir un excès.
2 Fe2+ + H2O2 + 2 H+ = 2 Fe3+ + 2 H2O
On a de l'acide chlorhydrique sous forme d'ions H+, les ions Cl- étant spectateurs.
Donc, pour chaque solution, il faut calculer combien de moles de Fe2+ il y a dans 10 mL.
Ensuite, calculer combien de moles il y a dans 1 mL d'acide chlorhydrique à environ 5 mol/L.
Ensuite voir si c'est suffisant...
Note bien qu'en fait, il suffit de le faire pour la solution J, les autres étant moins concentrées contiennent moins de moles de Fe2+.
1), 2) et 3) ->Ok
4)La quantité de matière de Fe2+ dans 10mL est en mol :
pour A: 3,6.10-7
B: 7,1.10-7
C: 1,1.10-6
D: 1,4.10-6
E: 1,8.10-6
F: 2,1.10-6
G: 2,5.10-6
H: 2,9.10-6
I: 3,2.10-6
J: 3,6.10-6
Tu trouves pareil? 
Par contre, la masse molaire de l'acide chlorhydrique est elle bien 36,5g/mol puisque M(H)=1,0 g/mol et M(Cl)=35,5 g/mol?
C'est bien ça mais de toute façon on en a pas besoin, la quantité de matière d'acide chlorhydrique dans 1mL à 5mol/L est de 5,0.10-3 mol
Par contre quel calcul faire ensuite? vérifier que 2n(Fe2+)=2n(H+)? Ca ne marche pas d'après mes calculs.
Pour Fe2+, on a 20 mg/L pour la solution J. On prend 10 mL ==> 20.10-3 x 10-2 = 2.10-4 g
2.10-4 / 56 = 10-4 / 28  3,57.10-6 mol
3,57.10-6 mol
Pour HCl, on a 1 mL à 5 mol/L ==> 5.10-3 mol comme tu l'as écrit.
D'après l'équation, on doit avoir autant de moles de HCl que de Fe2+.
Donc le minimum pour HCl est donc 3,57.10-6 mol. 5.10-3 étant très supérieur à 3,57.10-6, il y a suffisamment de HCl pour que la réaction se produise (HCl est en excès).
4)La quantité de matière de Fe2+ dans 10mL est en mol :
pour A: 3,6.10-7
B: 7,1.10-7
C: 1,1.10-6
D: 1,4.10-6
E: 1,8.10-6
F: 2,1.10-6
G: 2,5.10-6
H: 2,9.10-6
I: 3,2.10-6
J: 3,6.10-6
OK
La 5 sert à savoir combien de moles il y a pour H2O2.
Pour une eau oxygénée à 10 volumes, on a 10 litres de dioxygène pour 1 litre d'eau oxygénée, dans les conditions normales.
2 H2O2  O2 + 2 H2O
O2 + 2 H2O
10 litres de dioxygène ==> 10 / 22,4 = 1 / 2,24 mol
Il y a le double de nombre de moles pour H2O2 ==> 1 / 1,12 mol/L
Petite précision dans le sujet de l'exo j'avais écrit "sur ma feuille de papier millimétré je trouve une concentration en ions ferreux de 2,2 mg/L qui correspond à l'absorbance de 0,121 du vin blanc. Ca me parait peu." Qu'en penses tu ?
Je regarde ce que tu as écrit 
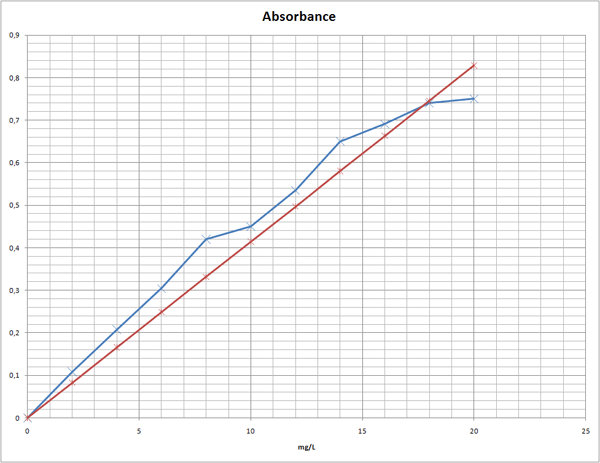
Oui, ça paraît peu effectivement mais si tu as mesuré une absorbance de 0,121, cela correspond effectivement à 2,2 mg/L ou 2,4 au grand maximum si on lisse la courbe.
Si c'est effectivement la valeur que tu as mesurée, on n'y peut rien. Il n'y a pas beaucoup d'ions ferreux donc pas de "casse ferrique".
Ce qui me gêne davantage, c'est la 8 :
Comparer les deux mesures obtenues et commenter
Il y a deux mesures ?
Moi aussi ça me gène. Je ne l'ai pas mis mais dans l'énoncé après "Mesurer l'absorbance de la solution issue du vin blanc et utiliser le résultat obtenu pour déterminer la concentration en fer dans le vin blanc." il y a "faire une mesure à l'oeil mais je ne comprends pas ce que ça veut dire (je ne l'ai pas fait lors du TP  ), cela doit être la deuxième mesure
), cela doit être la deuxième mesure
En fait, la mesure à l'il consiste à rechercher duquel des tubes de l'échelle de teintes se rapproche le plus le tube du vin. Je ne l'ai pas fait, afin de l'exo je propose de choisir un des tubes, le F ou le G?  ...
...
Pour la question 4)
Il y a donc suffisamment de HCl pour que la réaction se produise dans chacun de tubes. Oui? 
J'ai refais la courbe (avec juste le début), je trouve une concentration en iosn ferreux de 2,2 mg/L pour le tube avec le vin, donc je dirais que c'est le tube G qui a la teinte la plus proche de ce tube.
faire une mesure à l'oeil
OK, il fallait comparer visuellement le tube contenant le vin aux différents tubes contenant les solutions de Fe2+ aux différentes concentrations.
C'est difficile à faire maintenant mais si la mesure que tu as faite est bonne, ce serait plutôt le tube A.
Ha oui le tube A ! Ok 
Mais, à quoi servent les quantités de matière de 15:12 au fait?
Il y a donc suffisamment de HCl pour que la réaction se produise dans chacun de tubes?

Je regarde la question 5)
je trouve une concentration en ions ferreux de 2,2 mg/L pour le tube avec le vin, donc je dirais que c'est le tube G qui a la teinte la plus proche de ce tube.
Le tube G a une concentration de 14 mg/L, pas 2,2 ...
Il y a donc suffisamment de HCl pour que la réaction se produise dans chacun de tubes
Oui
à quoi servent les quantités de matière de 15:12 au fait?
Elles servent à montrer qu'il y a suffisamment d'acide chlorhydrique mais, en fait, il suffit de prendre la plus grande concentration c'est-à-dire la solution J. Si c'est vrai pour la solution J, c'est vrai pour les autres puisque les quantités de matière sont plus faibles.
Donc en fait c'est pas parceque 5.10^-3>3,57.10^-6 que la quantité est suffisante mais parceque 3,6.10^-6>3,57.10^-6 non? Je nage.
je trouve une concentration en ions ferreux de 2,2 mg/L pour le tube avec le vin, donc je dirais que c'est le tube G qui a la teinte la plus proche de ce tube.
Oui oui c'est n'importe quoi, en plus au lieu d'écrire 2,4 mg/L j'ai remis 2,2 mg/L

Donc 2,4 mg/L avec la courbe

J'ai fait un graphique aussi.
J'ai fait une régression linéaire pour lisser la courbe (droite rouge).
Donc en fait c'est pas parceque 5.10^-3>3,57.10^-6 que la quantité est suffisante mais parceque 3,6.10^-6>3,57.10^-6 non?
Pour que la réaction soit complète, il faut au minimum 3,57.10-6 moles puisqu'il faut autant de moles de HCl que de moles de Fe2+.
Comme on a 5.10-3 moles de HCl, on en a beaucoup plus qu'il nous en faut (5.10-3 > 3,57.10-6). On a donc du HCl en excès.
La 5 sert à savoir combien de moles il y a pour H2O2.
Pour une eau oxygénée à 10 volumes, on a 10 litres de dioxygène pour 1 litre d'eau oxygénée, dans les conditions normales.
2 H2O2 O2 + 2 H2O
O2 + 2 H2O
10 litres de dioxygène ==> 10 / 22,4 = 1 / 2,24 mol
Il y a le double de nombre de moles pour H2O2 ==> 2(1 / 2,24) = 1 / 1,12 mol/L
Une goutte faisant 0,05 mL, 10 gouttes vont faire 0,5 mL.
Donc, dans 10 gouttes de H2O2, il y a (1 / 1,12)5.10-4 = 5.10-4 / 1,12  0,446.10-3 mol.
0,446.10-3 mol.
D'après la réaction, il faut 3,75.10-6/2 = 1,875.10-6 moles de H2O2.
Donc, comme 0,446.10-3 > 1,875.10-6, il y a suffisamment de H2O2. H2O2 est en excès aussi.
Oui mais on compare les quantités de matière des différentes solutions avec rien du coup
On compare à chaque fois avec 5.10-3
solution A : 3,6.10-7 moles de Fe2+ donc il faut 3,6.10-7 moles de HCl. Et on a 5.10-3 de HCl, donc largement ce qu'il faut...
solution B : 7,1.10-7 moles de Fe2+ donc il faut 7,1.10-7 moles de HCl. Et on a 5.10-3 de HCl, donc largement ce qu'il faut...
etc...
solution J : 3,6.10-6 moles de Fe2+ donc il faut 3,6.10-6 moles de HCl. Et on a 5.10-3 de HCl, donc largement ce qu'il faut...
Mais, comme je l'ai dit, il suffit de le faire avec la solution J puisque les autres solutions ont moins de quantité de matière. Donc, si c'est bon avec J, c'est bon pour les autres solutions.
Je pense qu'il ne faut que deux chiffres significatifs à 3,57 mol soit 3,6 mol non?
Oui, tu fignoles ce genre de détail. Ce que je veux te transmettre, c'est surtout le principe de résolution.
Pour la 6, le principe est le même :
Fe3+ + SCN-
 FeSCN2+
FeSCN2+
Il y a autant de moles de Fe3+ que de moles de Fe2+ ( 2 Fe2+ + H2O2 + 2 H+ = 2 Fe3+ + 2 H2O )
Pour que la réaction soit complète, il faut autant de moles de SCN- que de moles de Fe3+.



