Inscription / Connexion Nouveau Sujet
Formule conductivité ion polychargé
je veux savoir la formule exacte de la conductivité d'un ion polychargé comme SO4^2- et Ag^2+
***Titre modifié***
Bonjour quand même, c'est la moindre des choses quand on s'adresse à des êtres humains (même sur un forum).
Ensuite, ce n'est pas "je veux" mais "je voudrais" : il n'y a en effet aucune obligation de réponse
désolé
bonjour
si on a une reaction comme ça
Ag2SO4 ----> 2Ag+ + SO4 (2-)
Alors la conductivité :
Sigma (Ag2SO4) = Sigma (Ag+) + sigma(SO4 (2-))
sigma (SO4(2-)) = [C] * lambda(SO4(2-))
on multiplie pas par le nombre de charge qui est 2 ???
Attention, un composé ionique solide est électriquement neutre, on ne peut pas parler de conductivité, ce qui n'est valable que pour les ions présents en solution.
La conductivité d'une solution S s'écrit :
Après il va falloir exprimer les concentrations en ions argent et sulfate en fonction de la concentration molaire C de la solution.
Pour ce faire, utilise l'équation de dissolution écrite ci-dessus pour les déduire.
merciiii .
j'ai une petite question , j'ai cherché un peu et j'ai trouvé une formule de conductivité d'une solution :
 =
= 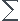 [Ci]
[Ci] 
 i
i  zi
zi
le zi c'est le nombre de charge de l'ion .
je suis vraiment bloqué toute la journé pour résoudre un exercice . est ce avec zi ou pas ....
voila est ce que tu peux me dire quelque chose à propos de ça ?
Je te déconseille fortement de retenir cette formule, sujette à interprétation.
Retiens celle-ci :
Ce qui aboutit pour une solution de sulfate d'argent à :
Exprimons les concentration en ions argent et sulfate en fonction de la concentration de la solution
:
- l'équation de dissolution du sulfate d'argent dans l'eau est
donc pour 1 mole de sulfate d'argent dissoute, il se forme 2 moles d'ions argent et 1 mole d'ions sulfate, soit
si est le volume de la solution
, qu'on peut simplifier dans la relation :
Finalement,
et
On peut ainsi reprendre la relation de la conductivité de la solution :


