Inscription / Connexion Nouveau Sujet
Diagramme de distribution d'un indicateur coloré
Bonsoir j'aimerais avoir de l'aide pour cet exercice :
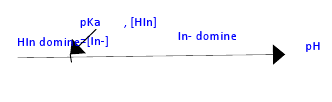
Un indicateur coloré acido-basique est un couple acido-basique Hlnd/Ind- dont les espèces conjuguées ont des teintes différentes. On considère une solution aqueuse de bleu de bromophénol, indicateur coloré acido-basique, de concentration molaire en soluté apporté C=mmol.L. La teinte de la forme acide Hlnd est jaune, celle de la forme basique Ind- est bleue. Une étude expérimentale permet de tracer le diagramme de distribution des formes acide et basique de l'indicateur coloré. Ce diagramme indique les pourcentages des formes Hlnd et Ind- en fonction du pH.
a) Identifier le graphe correspondant à la forme acide Hlnd et celui qui correspond à la forme basique Ind-.
b) En justifiant la démarche, déterminer à partir du graphe, le pKa du couple acido-basique Hlnd/Ind- associé à l'indicateur coloré.
c) Tracer le diagramme de prédominance du couple Hlnd//Ind-.
d) Quelle est la teinte de l'indicateur coloré dans une solution dont le pH prend successivement les valeurs 2,4 puis 9 ?
e) Exprimer les pourcentages P(Hlnf) et P(Ind-) en fonction de C, [Hlnd] et [Ind-]. En déduire les valeurs des concentrations [Hlnd] et [Ind-] lorsque le pH de la solution aqueuse vaut 3,5.
j'ai fait :
a) comment peut on le savoir
b) c'est le point d'intersection des deux courbes mais je dois prendre l'ordonnée ou l'abscisse pour prendre le pKa
j'ai du mal à faire le reste merci de m'aider 
salut  !
!
qui est l'acide ? qui est la base ? Un acide est présent dans les pH faibles... Et une base dans les pH plus forts.
Tu as le pKa ?
l'acide est Hlnd et la base Ind- donc la base est bleue et l'acide rouge ?
non justement je n'ai pas le pKa
Oui c'est bien ça pour l'attribution des courbes
b) A pH=pKA, l'acide et la base d'un couple ont la même concentration, c'est donc à l'intersection des 2 courbes que tu lis le pKa sur l'axe des abscisses
ouaip c'est bien ça 
c) fais une échelle de pH et place le pKa. Ensuite tu dis quelle espèce domine selon le pH
d) Pour pH = 2,4, tu es dans le domaine où l'acide du couple domine
Pour pH = 9 tu es dans le domaine où c'est la base du couple qui prédomine
D'après ton graphe tu vois que tu êux lier le pourcentage au pH. Quel est le lien entre le pH et le pKa ? Et entre ces données et les concentrations ?
ouais très bien.
Et entre le pH et les concentrations ? Ecris ton équation chimique et fais un tableau si tu as du mal
Hln + H2O = In- + H3O+
c = [Hln]eq + [In-]eq
Et pour pH = 4 tu as [Hln]eq = [In-]eq
Tu en déduis [ H3O + ] eq = 10-4 mol/L et dans ce cas Ka = 10-4
Or pour ce cas là tu as 50 % de chaque espèce
Tu as de quoi lier
Ben tu as déjà le lien entre c et les deux concentrations (je te l'ai donné)
Et les pourcentages de ces concentrations, c'est simplement les ramener sur 100
pKa = - log Ka
-log [Ka] = - log [H+] - log[A-]/[AH]
=> pKa = pH - log[A-]/[AH]
d'où la définition du pH en fonction du pKa :
pH = pKa + log[A-]/[AH]
? mais c'est bizarre ça j'pensais que t'avais fait une faute de frappe 
Dans ce cas tu dois vérifier que tu retrouves le rapport de proportion.
A partir de la formule liant le pH et le pKa, tu exprimes le rapport en fonction de ces données
Mais je sais, d'où ma première phrase 
Reprends la relation de 18h28 liant toutes les données. Imagine que les deux concentrations soient des inconnues (en + t'as même pas à l'imaginer elles le sont). Comment exprimes-tu ces concentrations en fonction de pH et pKa ?
Pour faire simple tu as pH = pKa + log([A-]/[AH])
=> log([A-]/[AH]) = pH - pKa
=> ([A-]/[AH]) = 10pH - pKa
Jusque là ça va ?
Ça te donne ([A-]/[AH]) = 0,32 en arrondissant à 10-2
Maintenant étant donné que tu ne connais pas C tu es obligée de garder une expression littérale.
Après tu peux lier ces deux concentrations et C à l'équilibre (post de 18h10) mais tu ne peux pas en faire plus
Bonjour à vous deux Manon 430 il me semble que tu as oublié que la concentration
En soluté apporté est de 20mmol/l ce qui permet je pense de débloquer l'exercice
PS: je le sujet à rendre !
Pourriez vous reprendre la dernière partie! S'il
Vous plaît !?