Inscription / Connexion Nouveau Sujet
Synthèse d'un savon
Bonjour, j'ai un petit problème concernant un exercice de chimie spé (matériaux). Je ne sais pas comment m'y prendre, si quelqu'un peut me donner quelques pistes ce serai super ! Merci beaucoup et bonne journée !
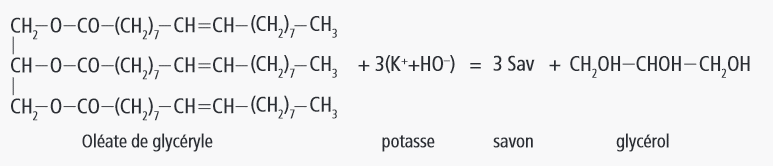
Comme données, j'ai l'équation de la réaction de synthèse d'un savon que j'ai joint en image, ainsi que les masses molaires atomiques :
C:12,0
H:1,0
O:16,0
K:39,1
A partir de cela on me demande : Est-il possible d'obtenir 900 kg de savon Sav par la saponification de 884 kg de
cette huile végétale ?
Bonjour brembo21 :
Masse moléculaire de l'oléate de glycéryle : C57H104O6 = 884
Masse moléculaire de l'oléate de potassium ( savon ) = C18H33KO2 = 320 .
884 kg ( 1000 mol ou 1 kmol ) d'huile végétale .
Dans l'équation , tu vois que 1 mole d'oléate de glycéride ( 884g ) , va donner 3 moles de savon ( 3 x 320 = 960g ) .
Donc c'est possible . Bonnes salutations .



