Inscription / Connexion Nouveau Sujet
Ph
Bonjour j'ai une question et j'ai bcp de mal pouvez vous m'aidez ?
Alors voilà montrer que avant l'équivalence le ph de la solution après un ajout de volume Vb de solution titrante s'exprime par
Ph= pKa+ log (Cb.Vb)/(Ca.Va -Cb.Vb)
Cb.Vb c'est [HO-] et Ca.Va c'est [C2H4O2]
Salut,
pH = pKa + log [base]/[acide]
[base]= n base/Vtot = CbVb/(Va+Vb)
[acide]= n acide/Vtot =(CaVa-CbVb)/(Va+Vb)
donc [base]/[acide]=CbVb/(CaVa-CbVb)
Merci beaucoup. J'ai une autre question la voici : un indicateur de fin de reaction est utilisable en ph- metrie si sa zone de virage est entièrement contenu dans le sauf de ph. Justifier le choix de cet indicateur.
Merci. 
Salut,
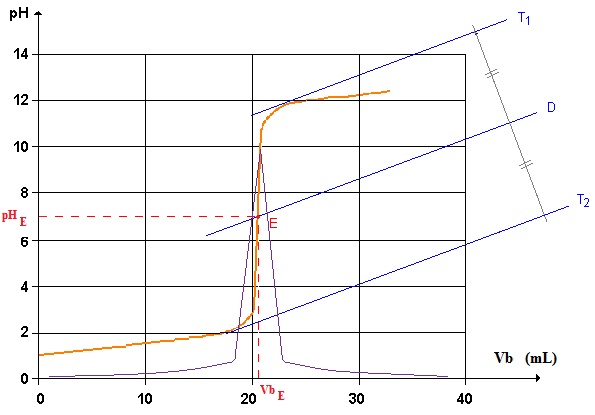
si tu visualise la courbe obtenue en faisant pH en fonction de volume versé, tu devrais voir qu'il y a une phase où le pH varie peu puis variation brusque puis de nouveau une variation faible.
Le saut de pH est la variation brusque.
ici comme tu verses de la soude dans un acide faible,
la 1ere zone calme s'arrête verss pH3 (c'est une supposition, je n'ai aucune donnée permettant de l'affirmer) et la 2e zone calme est peut-être au alentour de pH9
si c'est le cas il faut prendre un indicateur qui change de couleur entre 3 et 9 par exemple en truc qui vire entre 4 et 8