Inscription / Connexion Nouveau Sujet
Eliminations des ions nitrate par une résine échangeuse d'ions .
bonjour
J'ai des difficultés pour faire l'exercice suivant :
Les résines échangeuses d'ions peuvent être utilisées pour diminuer la concentration en ions nitrate d'une eau polluée. L'amberlite est une résine échangeuse d'anions constituée d'un réseau de polystyrène sur lequel sont gréfés des groupes ammonium -NH+3. La résine est initialement chargée en ions chlorure et est notée : R-NH+3, CI(-).L'étape de préparation de la résine permet de charger la résine en ions hydroxyde., Pour cela, on fait passer une solution d'hydroxyde de sodium (NA(+), HO[-))jusqu'à l'obtention d'une solution basique en sortie de colonne . La résine est prête et notée : R-NH (+)(3),HO(-)
1
a : On peut qualifier l'Amberlite de résine échangeuse d'anions. Expliquer
b : écrire l'équation de processus d'échange d'ions lors de la préparation de la résine.
c : La résine est constituée de billes de diamètre de l'ordre de 0.6 mm. Quel est l'avantage d'un matériau finement divisé ?
d : Pourquoi dit-on que la résine est prête lorsque la solution est basique en sortie de colonne ?
2
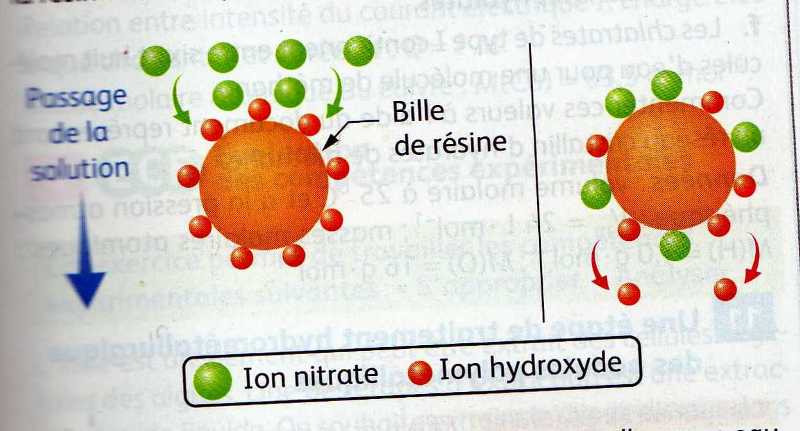
On fait passer, sur la résine chargée, un volume V=10.0 mL d'une solution inconnue, puis environ 100 mL d'eau distillée. Le liquide est recueilli dans un erlenmeyer en sortie de colonne. On considérera que tous les ions nitrate ont été échangées sur la résine selon le processus décrit par le schéma ci-dessous.
a : Expliquer comment la résine permet de dépolluer une eau.
b : Ecrire l'équation du processus d'échange se déroulant dans la résine.
c : Quels sont les ions présents dans l'erlenmeyer ?
3
On dose le liquide recueilli dans l'erlenmeyer à l'aide d'acide chlorhydrique (H3 O[sup]+, CI-)de concentration c[sub]A= .0100 mol.L-1. L'équivalence du titrage est repérée lorsque le bleu de bromothymol passe brusquement du jaune au vert. Le volume à l'équivalence est Ve= 13.4 mL.
a : Ecrire l'équation de la réaction support de titrage.
b : Déterminer la concentration molaire c de la solution de nitrate de potassium.
Mes réponse :
1)a)
b)
c) Il permet d'arreter de fin élément
d)
2 a)Car la résine "attrappe" les ions nitrate qui pollue l'eau .
b)
c) on a la précense d'ions hydroxyle dans l'erlenmeyer .
Pouvez me donner des pistes piste pour que j'essaie de la résoudre par moi même ?
Merci d'avance 
salut  !
!
1) a) au début tu as des ions chlorures puis tu as des ions hydroxydes
b) à voir avec la question précédente
c) oui
2) a) oui
b) voir la question 1b) c'est la même chose
c) oui
3)
3
On dose le liquide recueilli dans l'erlenmeyer à l'aide d'acide chlorhydrique (H3 O+, CI-)de concentration cA= .0100 mol.L-1. L'équivalence du titrage est repérée lorsque le bleu de bromothymol passe brusquement du jaune au vert. Le volume à l'équivalence est Ve= 13.4 mL.
a : Ecrire l'équation de la réaction support de titrage.
b : Déterminer la concentration molaire c de la solution de nitrate de potassium.
des idées ?
3) Si le produit de l'equation dans le eux est bon , je peux utiliser le titrage
A l'équialence No= N1
Donc Ca*Va= c*Ve où ca= 0,100 mol.L-1 Va= 1OO+10= 110 ml et Ve= 13,4 ml
c=( CA* Va)/ Ve
C'est l'équation de réaction à 17 h 29
NH3+, Cl- + Na+,OH- --> NH3+, OH-
Car lorsqu'on mélange la résine initialement chargé en chlorure (NH3+, Cl- ) avec une solution d'hydroxyde de soduim (Na+,OH-) --> cela nous donne la resine prête (NH3+, OH-)
Faut-il que je rejoute le R- devant ? Si j'ai fait faux où sont les erreurs ?
dans l'équation du 2 b) , c'est quelle resine qui est pris en compte , celle cargé en ions chlorrure ou en ions hydroxyde ?
On considérera que tous les ions nitrate ont été échangées sur la résine selon le processus décrit par le schéma ci-dessous.
donc prends le schéma, c'est l'échange nitrates-hydroxydes que tu veux

tu le sors d'où ton potassium là ?
Le produit n'est pas possible, modélise simplement l'échange d'ions 
ouais ok, pour moi ça ne venait qu'à la question 3 mais tu as l'énoncé sous les yeux donc ok 
Par contre O4-H ça n'existe pas


