Inscription / Connexion Nouveau Sujet
Compte rendu TP
Bonjour,
Alors voilà j'ai un compte rendu de TP a rendre pour mardi je demande votre aide =)
voici la feuille du TP :
** images effacées **
Dans la partie 1) Je n'arrive pas a faire ces deux questions :
Justifier le choix de cette longueur d'onde(voir spectre)
Etablir la relation entre l'absorbance A de la solution et sa concentration molaire
Voila pouvez vous m'expliquer merci d'avance
Edit Coll : si tu veux de l'aide, merci de faire l'effort de recopier ton énoncé sur le forum 
![]()
Bonjour
Une des règle du forum est d'ECRIRE SOIS MEME L'ENONCE !!! Tu ne peux donc pas mettre une image de l'énoncé (tu peux par contre mettre une image d'un diagramme ou d'un schéma).
OK?
Bonjour,
alors j'ai un compte rendu de Tp a rendre pour demain qui me parait difficile
Chaque binôme a en charge la préparation d'une solution de l'échelle de teinte:
On prépare les solutions filles du tableau qui suit à partir d'une solution mère d'iodure de potassium (K+(aq),I-(aq)) de concentration molaire c1=4.00E10-3Mol.L-1.
On indique également dans le tableau le volume de solution fille a préparer :
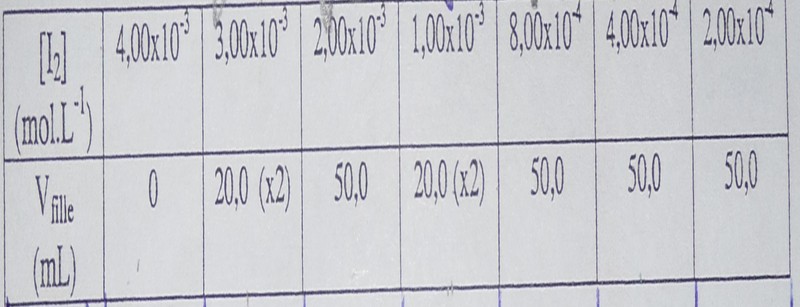
1)Tracer de la droite d'étalonnage
1A l'aide du spectrophotomètres mesurer l'absorbances A des 6 solutions.On travaille a la longueur d'onde lanbda=480 nm. reporter les mesures en ajoutant une ligne au tableau précédent.
Cette question est effectuer
2)Justifier le choix de cette longueur d'onde (voir spectre)
Je n'arrive pas a cette question
Partie 2 :
Pour cette transformation chimique la seule espèce colorée est le diiode I2.Sa formation au cours du temps est suivie par spectrophotomètre
On dispose des solutions aqueuses suivantes :
-solution d'iodure de potassium de concentration molaire c1=5.00E-1 Mol.L-1
-solution de peroxodisulfate de potassium de concentration molaire c2=1.00E-2 mol.L-1
On travaille a la longueur d'onde lanbda 490 nm.
questions
1) Ecrire les demi équations d’oxydoréduction associées au couples intervenant dans la réaction étudiée : S2O 82-/SO42- et I2/I-
En déduire l'équation de réaction
2e- + I2=2I-
2 e-+S2O 82- =2SO42-
Voici l’équation de réaction :
I2 + 2SO42- ----> 2I- + S2O 82-
2)Rappeler la relation littérale entre l'absorbance et la concentration molaire de la solution de diiode
U²= URC
3) En déduire la relation numérique pour la solution de diiode
4) Représenter en fonction de la courbe [I2]=f(t) en la déduisant de la courbe A=f(t)
5) Établir le tableau d'avancement pour cette réaction
6) Exprimer la concentration molaire en diiode à la date t en fonction de l'avancement x
7) Représenter en fonction du temps l'évolution de l'avancement de la réaction pour le volume de mélange préparé (V=20.00 mL)
Donc voila ce que j'ai a faire pour demain j'ai juste trouver la question 1 et 2 mais je ne suis pas sur des résultats a me confirmer après merci de m'expliquer les autres question svp merci d'avance
*** message déplacé ***
Edit Coll : image placée sur le serveur de l'  Merci d'en faire autant la prochaine fois !
Merci d'en faire autant la prochaine fois ! 
![]()
Bonjour,
alors j'ai un compte rendu de Tp a rendre pour demain qui me parait difficile
Chaque binôme a en charge la préparation d'une solution de l'échelle de teinte:
On prépare les solutions filles du tableau qui suit à partir d'une solution mère d'iodure de potassium (K+(aq),I-(aq)) de concentration molaire c1=4.00E10-3Mol.L-1.
On indique également dans le tableau le volume de solution fille a préparer :
** image effacée **
1)Tracer de la droite d'étalonnage
1A l'aide du spectrophotomètres mesurer l'absorbances A des 6 solutions.On travaille a la longueur d'onde lanbda=480 nm. reporter les mesures en ajoutant une ligne au tableau précédent.
Cette question est effectuer
2)Justifier le choix de cette longueur d'onde (voir spectre)
Je n'arrive pas a cette question
Partie 2 :
Pour cette transformation chimique la seule espèce colorée est le diiode I2.Sa formation au cours du temps est suivie par spectrophotomètre
On dispose des solutions aqueuses suivantes :
-solution d'iodure de potassium de concentration molaire c1=5.00E-1 Mol.L-1
-solution de peroxodisulfate de potassium de concentration molaire c2=1.00E-2 mol.L-1
On travaille a la longueur d'onde lanbda 490 nm.
questions
1) Ecrire les demi équations d'oxydoréduction associées au couples intervenant dans la réaction étudiée : S2O 82-/SO42- et I2/I-
En déduire l'équation de réaction
2e- + I2=2I-
2 e-+S2O 82- =2SO42-
Voici l'équation de réaction :
I2 + 2SO42- ----> 2I- + S2O 82-
2)Rappeler la relation littérale entre l'absorbance et la concentration molaire de la solution de diiode
U²= URC
3) En déduire la relation numérique pour la solution de diiode
4) Représenter en fonction de la courbe [I2]=f(t) en la déduisant de la courbe A=f(t)
5) Établir le tableau d'avancement pour cette réaction
6) Exprimer la concentration molaire en diiode à la date t en fonction de l'avancement x
7) Représenter en fonction du temps l'évolution de l'avancement de la réaction pour le volume de mélange préparé (V=20.00 mL)
Donc voila ce que j'ai a faire pour demain j'ai juste trouver la question 1 et 2 mais je ne suis pas sur des résultats a me confirmer après merci de m'expliquer les autres question svp merci d'avance
*** message déplacé ***
Edit Coll
Bonjour
1) non ce n'est pas cette réaction là c'est la réaction contraire qui a lieu car on te dit qu'on suit la formation de I2 par spectro. De plus tu as introduits au départ des I- et des ions S2O82- !
2) Je ne la connais pas sous cette forme ! C'est quoi U, R et C ? Tu es sur de toi ?
*** message déplacé ***


