Inscription / Connexion Nouveau Sujet
spectre d'absorption
Bonjour
J'ai un exercice sur les spectres d'absorption.
Voici l'exercice:
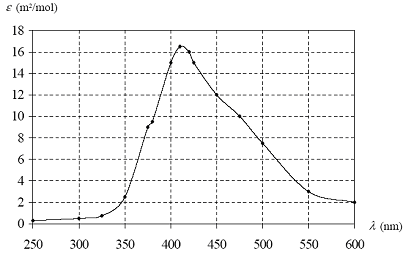
La courbe donnant le coefficient d'absorption molaire du dibrome gazeux est représentée ci dessous:
1 quelles sont les radiations absorbées par la vapeur de dibrome? Quelle est la couleur de cette vapeur?
2 La loi de Beer Lambert s'applique aussi aux espèce en phase gazeuse. Calculer l'absorbance maximale d'un flacon transparent contenant du dibrome gazeux sous la pression 25 Pa à 30°C. L'épaisseur traversée par le faisceau lumineux est de 5cm.
DOnc j'ai réussi la première question mais pour la deuxième je sais que je dois utiliser l'équation des gaz parfaits pour trouver la concentration pour pouvoir utiliser la formule de l'absorbance mais je n'arrive pas à trouver n.
Pouvez vous m'aider SVP?
PV = nRT tu a la température et la pression ou est ton probleme ??
tu pourrais essayer de remplacer n par CV  et sa devrait aller tout seul
et sa devrait aller tout seul 
( il te maquera quand meme une donné pour trouver l'absorbance max : epsilon le coefficient d'absortion du dibrome )
Je suis sur que tu n'a meme pas écrit ce que je t'ai conseillé... sinon tu ne dirais pas sa 
si j'ai lu ce que tu as écrit mais le V dans PV=nRT.
j'ai écris ça aussi 
tu pourrais essayer de remplacer n par CV
Bonjour,
Quelqu'un pourrait m'expliquer ceci ? Je suis sur le même exercice et je n'ai rien compris à vos explications...
Merci de votre aide


