Inscription / Connexion Nouveau Sujet
Solubilité et temperature (graph)
Bonjour,
J'ai un devoir maison de Physique Chimie qui d'après mon professeur doit être correctement rédigé...
J'ai même sur mon devoir maison les étapes à suivre pour rédiger qui sont :
-Introduire votre réponse
-Citer la formule sous forme littérale en l adaptant à la situation de l exercice
-Faire les conversions nécessaires
-Transformer la formule littérale en une formule numérique
-Réaliser le calcul
-Preciser l'unité du resultat
-S il vous ait demandé : Donner le resultat en ecriture scientifique avec le bon nombre de chiffres significatifs
-conclure votre resultat
Ainsi que la definition d'une écriture scientifique et d'un chiffre significatif
J'ai donc fait les exercices au brouillon (donc pas encore rédigé) mais je ne suis pas sûr de mes réponses et surtout de mes justifications...
Donc les exos (pour respecter les règles du forum je n'en mais qu'un sur ce topic) :
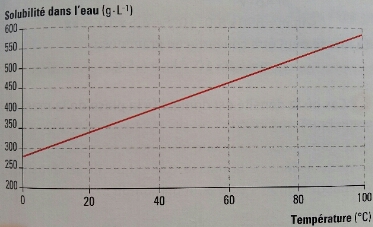
Le graph ci-dessous represente la solubilité du chlorure de potassium (KCI) dans l'eau en fonction de la température .
(Je vous envoi le graph dans mon prochain post)
1) comment évolue la solubilité en fonction de la temperature ?
2) 40g de chlorure de potassium sont introduits dans 100g d'eau à 25°C. La solution est elle saturée ? Si oui, quelle masse de chlorure de potassium n'est pas dissoute.
3) On desire obtenir une solution homogène. Pour cela, il est possible de chauffer le mélange precedent ou d augmenter la quantité d'eau.
a) A quelle temperature minimale faudrait il la chauffer ?
b) Quelle quantité minimale d'eau faudrait il ajouter ?
En ce qui concerne mes recherches, je les aies fait sur brouillon (donc pas redigée) :
1)Plus la temperature augmente, plus la solubilité augmente.
2) Graphiquement, la solution est saturée
Sur les 40g graphiquement, environ 35g est dissous, donc 40-35 égal un peu pres 5g de la solution reste sous forme solide au fond du bécher
3a) graphiquement : 40°C
b)Si 25°C
Je fais un produit en croix donc :
(35×111)÷40=97,125
Est ce bon s'il vous plait ?
Dois je justifier comme il est écrit sur mon DM ou une justification graphique suffit ?
Dans tout les cas est ce correctement justifié étant donné que mon professeur est tres exigeant ?
Merci 
Ps : les photos arrivent de suite
Re 
1) Oui. Mais encore ? Tu as une droite 
2) Il faut que tu détailles. Tu as un graphique solubilité en fonction de la température. Dans ta question on te donne uniquement la masse de KCl et ta masse d'eau. Tu dois dire comment tu trouves la solubilité
3) a) pareil que précédemment (mais ok)
b) Ok mais détaille. Attention un résultat sans unité ne vaut rien (sauf s'il est adimensionnel)
Ok merci donc,
Si j ai bien tout compris :
1) c'est aussi une fonction affine
2) Graphiquement la solution est saturée car elle dépasse les 350g/L^-1 soit une limite de 35g de chlorure de potassium pour une solubilité totale (cette expression est elle correcte? est ce tout pour cette justification ?)
400g/L^-1 represente 40g de chlorure de potassium, puisque seulement 35g peut etre dissous: 40-35 = 5g
Donc il ne reste que 5g solide au fond du bécher
Est ce correct ?
3)
A) graphiquement, pour 40g de chlorure de potassium (soit 400g/L^-1) il faut une temperature minimale de 40°C
Et pour le b)
Pour
35g j'ai 100g d'eau
40g j'ai x g d'eau
Donc je fais un produit en croix et je trouve un résultat en gramme...
Est-ce correct ?
Merci