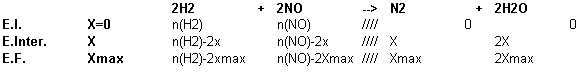Inscription / Connexion Nouveau Sujet
Réduction du monoxyde d azote par le dihydrogène
bonjour, Alors je dois déterminer l'état final de cette réduction (cf titre post)
je sais que cette réduction donne de l'eau et du diazote
les données sont les suivantes: :36 L ;
:43 L et
:20 L.mol-1
j'ai don équilibré l'équation : 2 NO+ 2 H 2 H
O + N
. j'ai calculé les nombres de moles pour chacun des composés n
= 1.3 mol et n
= 2.15 mol
Et je ne sais pas comment faire pour terminer...
merci de me répondre 

Bonjour 
En effet, tu as l'équation suivante.
pour avoir des infos sur l'état final, tu dois passer par le tableau d'avancement. Mais il te faut aussi des infos concernant les réactifs, ces infos tu les as.
ainsi tu as :
Ensuite, tu construits un tableau d'avancement. Détermine l'avancement maximal et en déduis les quantités de matière l'état final.
Tomm-Bou