Inscription / Connexion Nouveau Sujet
Quantité de matière
Bonsoir, j'ai contrôle de physique-chimie demain et le professeur nous a donné un exercice à faire en classe et il n'a pas eu le temps de le corrigé. Je voudrais savoir si vous pouvez m'expliquer comment faire s'il vous plaît ?
Donc je sais que n = m/M
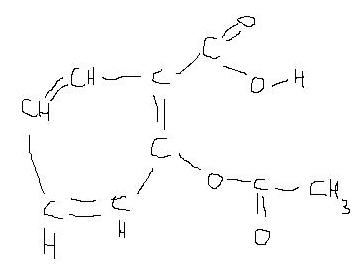
Quelle quantité de matière y-a-t-il dans 2 kg d'aspirine (voir formule développée, désolée pour la qualité mais dessiner la formule sur le logiciel paint ce n'est pas très facile)
donc 2kg = 2000g = m
Après je ne vois pas comment faire
Bonjour Emily64,
dans la formule de l'aspirine que tu donnes, il y a 9 atomes de carbone, 8 d'hydrogene et 4 d'oxygene. Sachant que la masser d'un atome-gramme de carbone est 12 g, celle de l'hydrogene 1 g et celle de l'oxygene 16 g, tu peux facilement calculer la masse molaire M de la molecule (M = 12x9 + 8 + 16x4, en grammes).
En divisant la masse de produit exprimee en g, soit 2000 g, par la valeur de M, tu obtiendras le nombre de moles d'aspirine contenues dans les 2 kg de produit.
Prbebo.



