Inscription / Connexion Nouveau Sujet
Probleme de Filtration et de solubilité
Bonjour,
J'ai un devoir maison de Physique Chimie qui d'après mon professeur doit être correctement rédigé...
J'ai même sur mon devoir maison les étapes à suivre pour rédiger qui sont :
-Introduire votre réponse
-Citer la formule sous forme littérale en l adaptant à la situation de l exercice
-Faire les conversions nécessaires
-Transformer la formule littérale en une formule numérique
-Réaliser le calcul
-Preciser l'unité du resultat
-S il vous ait demandé : Donner le resultat en ecriture scientifique avec le bon nombre de chiffres significatifs
-conclure votre resultat
Ainsi que la definition d'une écriture scientifique et d'un chiffre significatif
J'ai donc fait les exercices au brouillon (donc pas encore rédigé) mais je ne suis pas sûr de mes réponses et surtout de mes justifications...
Donc les exos (pour respecter les règles du forum je n'en mais qu'un sur ce topic) :
Un élève souhaite déterminer experimentalement la solubilité du sulfate de cuivre à 20°C.
Il introduit 40 g de sulfate de cuivre dans un bécher contenant 100,0 mL d'eau à 20°C et agite. Il observe que pour une masse de 40g de solide, la solution est saturée et du solide non dissous se depose au fond du bécher.
1)Dessiner le bécher apres agitation
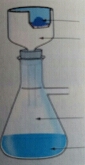
2) a) le melange hétérogène est filtré sur un Büchner. Recopier et compléter le schéma ci-contre en situant en particulier le sulfate de cuivre solide, le solvant et le sulfate de cuivre dissous.
b) Le filtrat est-il saturé ? Justifier.
3) La masse de sulfate de cuivre solide sec récupéré grâce au Büchner est de 4g. Quelle masse de solide a été dissoute dans les 100mL d'eau ?
4) En déduire la solubilité du sulfate de cuivre en g.L^-1 à 20°C
Avant de commencer, je tiens à preciser que pour l'exercice 4) dans le g.L^-1
Le . ne se situe pas tout en bas mais au milieu verticalement, et je ne sais pas ce qu'il represente.
Si vous pouvez me le dire, merci.
En ce qui concerne les exos, j'ai fait ceci au brouillon (donc pas redigé) :
1) photo dans mon second(ou deuxième ) post
2)a) IDEM
b) La solution etant déjà saturé, le filtrat ne peut etre donc que saturé... le mélange etant heterogene, le filtrat a seulement separer les deux phases...
3) 40g - 04 g = 36g
4) 1L = 1000 mL
1000ml/100
36g.L^-1 × 10 = 360 g.L^-1
Donc,
Est ce correcte s'il vous plait ?
Mes justifications aussi ?
Je n'arrive pas à trouver pour le 3) et 4) les formules à utilise, pouvez vous m'aider ?
Merci 
(J envoie les photos dans mon second (ou deuxieme si probleme) post car j'ai des problemes avec l envoi de photo de ce site
Les photos :
I ere image:
L image de l exo
2eme photo
Mon dessin brouillon pour l exo 2)a)
3eme photo
Mon dessin brouillon pour le 1)
J'ai du mal à voir la netteté des photos comme je suis sur smartphone mais j'espère que c'zst lisible...
Merci 

Salut 
1) ok
2) a) je n'y vois pas très bien mais ça semble ok
b) oui
3) oui mais marque ton raisonnement littéralement. Explique juste ce que tu as fait
4) pour le point c'est juste de la typo de la part de l'éditeur de pense car il s'agit bien de grammes par litre ici
Il faut que tu explicites, en l'état on ne comprend pas ce que tu as fait
Ok merci donc si j'ai bien tout compris :
2a) Je m'excuse je vais essayer de reenvoyer une autre photo plus nette
3) que 4g a été récupéré dans le Büchner. Le reste ayant été dissous, 40g (masse de sulfate de cuivre au départ) - 4g = 36g de solide qui a été dissout.
Est ce correcte vis a vis de la justification et la rédaction ?
La méthode de rédaction se trouvant dans mon sujet de DM, je me suis dit qu'il faut l'appliquer mais comme il n'y a je pense, pas de formule...
4) Etant donné que dans 100,0 ml d'eau à 20°C
36g de sulfate de cuivre est dissous, la formule pour determiner la solubilité à 1L d'eau à 20°C est :
g/L^-1×10
Soit
36g/L^-1 × 10 = 360g/L^-1
Est ce correctement justifié et est ce que je respecte bien les etapes à suivre pour la redaction ?
De même pour les chiffres significatifs avec lesquels je m'embrouillent souvent.
Merci 
3) oui c'est mieux. Il faut juste exposer son raisonnement de manière claire
4) heu non, tu ne dis pas pourquoi pas dix
Ok merci, en revanche je ne peux pas reenvoyer une autre photo pour l'exo 2a) 
Est ce bien rédigé comme ça ?
J'ai moyennement suivi les étapes à suivre dans mon DM mais je ne pense pas non plus qu'ils s'appliquent vraiment dans cet exercice puisqu'il n'y a, je crois, pas de formule.
4) Etant donné que dans 100,0 ml d'eau à 20°C
36g de sulfate de cuivre est dissous , il faut pour trouver la solubilité du sulfate de cuivre en g/L^-1, trouver le coefficient
(ce mot "coefficient" est il approprié dans cette réponse ?)
permettant de passer de la masse par 1000mL à la masse proportionnelle à celle precedente par 1L
1L= 1000mL
1000mL/100 = 10
Le coefficient trouvé, nous pouvons donc déduire la solubilité du sulfate de cuivre qui est de :
36g/L^-1×10=360 g/L^-1


