Inscription / Connexion Nouveau Sujet
physique gaz parfait
Bonjour,
Pouvez vous me corriger svp :
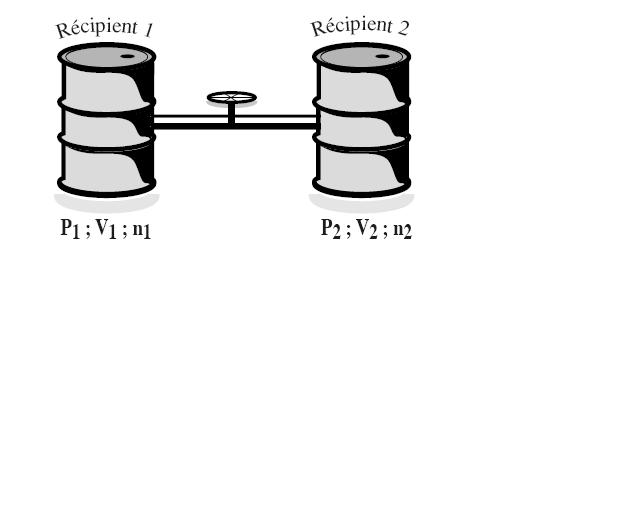
Deux récipients sont reliés par un tube de volume négligeable muni d'un robinet (voir schéma).
Ces deux récipients contiennent un gaz considéré comme parfait. La température de 27 °C ne varie pas pendant l'expérience.
La pression P1 et le volume V1 du récipient 1 sont respectivement : 2,0.10^5 Pa et 2,0 L
La pression P2 et le volume V2 du récipient 2 sont respectivement : 1,0.10^5 Pa et 5,0 L
Données : R = 8,31 S.I
1)Exprimer et calculer les quantités de matière n1 et n2 de gaz dans chaque récipient.
==> il faut utiliser l'équation d'état des gaz parfaits
PV = nRT
n1 = P1V1/(RT) avec V1 = 2 10-3 m3 et T =273+27 = 300 K
n1 =2 105*2 10-3 / (8,31*300)=0,16 mol.
n2 = P2V2/(RT) avec V2 =5 10-3 m3 et T =273+27 = 300 K
n1 =1 105*5 10-3 / (8,31*300)=0,2 mol.
2) On ouvre le robinet.
En déduire le volume total VT occupé par le gaz.
==> Volume total Vt occupé par le gaz. = V1 + V2= 7 10-3 m3.
La quantité de matière présente est n = n1 + n2 = 0,16+0,2 = 0,36 mol.
3)Déterminer PT, la pression du gaz lorsque le robinet est ouvert.
==> La pression finale est Pf = nRT/Vt = 0,36*8,31*300 /7 10-3 =1,28 105 Pa.
Merci