Inscription / Connexion Nouveau Sujet
identification d'ions en solution
Bonjour,
en cours nous avons fait un exercice que je n'ai pas réellement compris.
Le voici :
On dispose de 4 tubes à essais contenant des solutions ioniques différentes. Ces tubes nommés A, B, C et D ont été intervertis malencontreusement avant d'être étiquettés. Le but des expériences suivantes est de retrouver la solution ionique d'origine présente dans les tubes correspondants.
Les quatre composés ioniques sont :
- du chlorure de zinc ZnCl2
- du sulfate de cuivre CuSO4
- du chlorure de cuivre CuCl2
- du sulfate de fer FeSO4
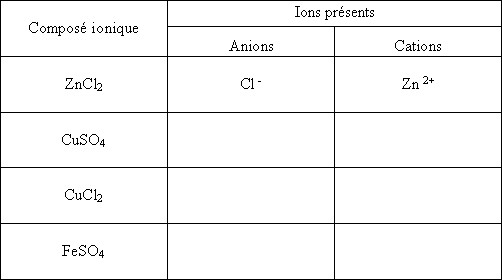
1°) Pour chaque composé ionique, donner les ions présents en solution en recopiant et complétant le tableau.
Comment trouver ce qu'il faut mettre dans le tableau ? Je ne comprends pas. Si quelqu'un a le temps de m'expliquer se serait avec plaisir 
Bonsoir Charlenou!
Tu dois simplement trouver quels sont les ions constituant les composés ioniques.
Pour ZnCl2, chlorure de zinc, tu as 2 atomes de chlore pour un atome de zinc. Donc tu as un ion Zn2+ et un ion Cl-.
Pour CuSO4, sulfate de cuivre, tu as autant d'ions sulfate que d'ions cuivre.
La formule de l'ion sulfate est SO42- et celle de l'ion cuivre II Cu2+.
Pour CuCl2, chlorure de cuivre, tu as comme pour le premier. Cu2+ et Cl-.
Pour le sulfate de fer FeSO4 c'est comme pour le second: SO42- et ion fer II Fe2+.
Il suffit que tu connaisses la formule des principaux ions et le tour est joué
J'explicite davantage ou l'explication te convient?
Ah, c'est bon j'ai compris comment trouver  il faut que j'apprenne la formule par coeur !
il faut que j'apprenne la formule par coeur !
Comment savoir si c'est Anion ou Cation ?
En général ça se voit dans la formule mais le mieux c'est que tu apprennes certains ions. la plupart des ions métalliques sont des cations


