Inscription / Connexion Nouveau Sujet
Exercice pourcentage massique d'un alliage en laiton
 ForbagROYAL
ForbagROYALBonjour, j'ai un exercice que je ne comprend pas, enfin si la moitié je connais mais pas la dernière :
Le laiton est un alliage de cuivre et de zinc. La composition de cette alliage doit être adapté à l'usage auquel il est destiné. Pour déterminer la composition en masse d'un étang, à un échantillon est introduit dans l'acide chlorhydrique concentré : le Zinc réagit avec lion H+(aq) de l'acide, pour former lion zinc Zn2+ (as) et du dihydrogène H2 (g). Le cuivre ne réagit pas avec l'acide chlorhydrique.
Un échantillon de l'étang de masse m = 2,90 g est placé dans une grande quantité d'acide chlorhydrique
- en déduire la composition massique de l'alliage étudié...
Ok bon déjà pour répondre à celui ci j'ai fais ces deux questions :
Dans les conditions de l'expérience, on recueille un échantillon de volume V = 0,32 litre de d'hydrogène.
La masse du graphic indique 0,9 g et le cuivre j'ai trouvé 2g car 2,90-0,9.Bon je sais qu'il réagit pas avec l'acide chlorhydrique, mais j'ai pas du tout l'idée.
De plus j' ai voulu faire un produit en croix mais il me manque un certain pourcentage, je trouve pas le fameux chiffre pour le débloquer  .
.
Pas de réponse ! Juste que des indices.
Merci d'avance
Bonsoir ForbagROYAL,
Il faudrait que tu recopies fidèlement ton énoncé d'exercice car j'ai l'impression que tu nous as fourni que des bribes.
S'il y a un schéma de l'expérience, tu peux le joindre à la recopie.
Effectivement il y'avait la photo ci dessous et deux autres questions trouvés :
recopier et compléter l'équation de la réaction modélisant la transformation entre le zinc et l'acide chlorhydrique.
Et
Citer un test permettant de caractériser le gaz produit lors de cette transformation
Mais je pense pas qu'il y'est pas grande utilité à ceux là.
Il y a une règle d'or sur un forum, c'est ne pas croire qu'abréger ou reformuler un énoncé d'exercice peut faire gagner du temps à tout le monde, c'est généralement le contraire 
La première étape consiste à écrire l'équation-bilan de la transformation chimique.
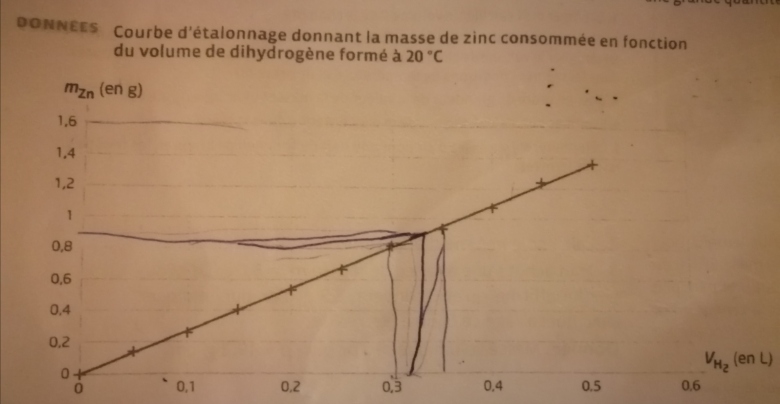
Pour V(H2) formée, il semble effectivement que la masse de zinc consommée soit m(Zn) = 0,9 g
Il faut donc maintenant faire un bilan de matière à l'état initial et à l'état final, à l'image de ce qui est fait dans la fiche suivante ![]() Les transformations chimiques
Les transformations chimiques

Il faut que tu présentes bien les choses dans ce type d'exercice :
Etape 1 : écrire l'équation-bilan de la transformation
Etape 2 : faire le bilan à l'état initial
Etape 3 : faire le bilan à l'état final.
En gros, je ne dis pas que tu ne l'as pas fait, je te dis juste qu'il faut améliorer ta rédaction  .
.
En effet, tu es désormais au lycée et c'est ce qu'on te demandera lors du bac, autant donc s'entraîner de suite.
Une remarque en passant sur la recopie de l'énoncé :
Une relecture avant envoi est plus que souhaitable.
Cela éviterait, par exemple, de transformer
" un échantillon de laiton " avec " un échantillon de l'étang "
Le correcteur d'orthographe, non surveillé, peut jouer de mauvais tours.


