Inscription / Connexion Nouveau Sujet
Etude de l'étiquette d'un médicament, le Timoferol
Bonjour !
Dans un DM pour la rentrée, je dois répondre à ces questions :
Voici les données
Composition par gélule Sulfate ferreux 172,73 mg soit fer : 50 mg
Acide ascorbique (vitamine C) 30 mg Magnésium carbonate E504 Talc E553b Silice E551 Amidon de mais Enveloppe de la gélule : Gélatine
Titane dioxyde E171 Bleu patenté V E131 Jaune de quinoléine E104
Quels sont les principes actifs et les excipients de ce médicament ? Justifier.
Selon moi, les principes actifs sont le sulfate ferreux et l'acide ascorbique, les excipients tout le reste.
A quoi sert la vitamine C dans ce médicament (son ou ses rôle-s) ?
Elle favorise l'absorption du fer par l'intestin, ce qui combat l'anémie, et empêche son oxydation.
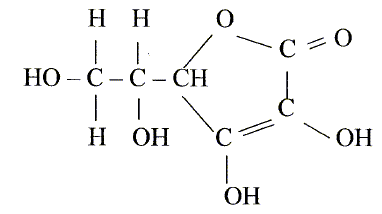
Quels sont les groupes caractéristiques de la formule développée e la vitamine C ?
J'ai trouvé les groupes carboxyle et hydroxyle.
Masse molaire moléculaire de l'acide ascorbique ?
(6*12)+8+(6*16)=M= 176 g/mol
Quantité de matière d'acide ascorbique dans une gélule ?
Acide ascorbique dans une gélule= 30 mg= 0,030 g= m
0,030/176= 1,7*10-4 mol= n
Sulfate ferreux 172,73 mg
Masse molaire du sulfate ferreux ?
(1*55,8)+(1*32)+(4*16)=151,8 g/mol= M
Quantité de matière de sulfate ferreux contenue dans une gélule ?
0,17273/151,8=0,001 mol
Expliquer "soit fer : 50 mg"
Là, je bloque, je ne comprends pas du tout.
Merci beaucoup.
Quels sont les principes actifs et les excipients de ce médicament ? Justifier.
les principes actifs sont le sulfate ferreux et l'acide ascorbique , les excipients le reste
A quoi sert la vitamine C dans ce médicament (son ou ses rôle-s) ?
Ce médicament contient du fer, élément minéral essentiel au fonctionnement de l'organisme. Le fer est indispensable à la formation de l'hémoglobine, contenue dans les globules rouges, qui assure le transport du dioxygène dans le sang. Il est utilisé dans le traitement des carences en fer responsables de certaines formes d'anémies.
La vitamine C est une vitamine hydrosoluble (soluble dans l'eau) C'est un puissant anti-oxydant qui joue un rôle essentiel dans de nombreux processus vitaux :
- Elle freine le vieillissement des cellules
- Elle favorise l'entretien des tissus
- Elle accélère la cicatrisation
- Elle augmente la résistance aux infections
- Elle combat l'anémie en favorisant l'absorption du fer par l'intestin
Quels sont les groupes caractéristiques de la formule développée e la vitamine C ?
ci joint la formule développé de la vitamine C
groupe -OH =>hydroxyle
groupe -C=O => carbonyle
Masse molaire moléculaire de l'acide ascorbique ?
(6*12)+8+(6*16)=M= 176 g/mol oui
Quantité de matière d'acide ascorbique dans une gélule ?
Acide ascorbique dans une gélule= 30 mg= 0,030 g= m
0,030/176= 1,7*10-4 mol= n
oui, c'est bon
Sulfate ferreux 172,73 mg
Masse molaire du sulfate ferreux ?
par contre on ne te dit pas s'il est hydraté. On va vide que non (sinon on te l'aurait indiqué)
sulfate ferreux => FeSO4
masse molaire = 55.8+32+4*16 = 151.8 g/mol
Quantité de matière de sulfate ferreux contenue dans une gélule ?
Bonjour !
Donc, tu trouves 63 mg pour la dernière question "Expliquer soit fer : 50 mg" ? Comment as-tu fait ?
Dans tous les cas, merci beaucoup. Je te souhaite un excellent réveillon et une bonne année 2012 !


