Inscription / Connexion Nouveau Sujet
DM chimie
Bonjour, j'ai un problème dans un Dm de chimie dont l'énoncé est:Bonjour, j'ai un exercice ou je bloque sur quelque question merci de m'aider
exercice:
Sur le plateau d'une balance, on place une capsule contenant 0,84g d'hydrogénocarbonate de sodium solide (NaCHO3), un flacon contenant un volume V d'acide chlorhydrique (H+(aq)+Cl-(aq)) et son bouchon. L'ensemble constitue un système chimique dans son état initial et l'on note m1 sa masse. On verse l'hydrogénocarbonate de sodium dans le flacon, que l'on bouche. On observe une effervescence et on attend que celle-ci cesse. On ouvre alors le flacon et on note la masse m2 de ce nouvel ensemble. L'experience est réalisée trois fois:
VolumeVd'acidechlorhydrique-Masse m1-Masse m2
expérience 1 50ml 90,84g 90,62g
expérience 2 100ml 140,84g 140,4g
expérience 3 150ml 190,84 190,4g
La transformation se produisant est une réaction entre l'ion hydrogénocarbonate HC03- contenu dans le solide et les ions H+(aq) de l'acide.
Questions :
1. L'effervescence trouble l'eau de chaux. En déduire la nature d'un des deux produits de la réaction.
2. En ajustant l'équation chimique de la réaction, déterminer l'autre produit de la réaction.
3. Pour chacune des experiences, déterminers la masse de CO2 formé.
4. En comparant la composistion des réactifs et celle des produits , déterminer, pour chacun des systèmes, le réactif en excés(celui qui n'est pas totalement consommé).
5. En déduire de quel réactif dépend la quantité de produit formé.
J'ai répondu aux 3 premières mais je n'arrive pas à faire les deus dernières.
Si quelqu'un pouvait m'aider, ce serait gentil.
Merci à ceux qui voudront bien m'aider
salut  !
!
Pour pouvoir t'aider il faudrait que je puisse corriger les trois premières, histoire de savoir si tu pars sur de bonnes bases.
Sinon
4) tu fais un tableau d'avancement
Déjà, merci de me répondre
Pour la 1) L'effervescence trouble l'eau de chaux donc il y a du CO2
2) L'équation est HCO3-+H+->CO2+H2O
l'autre produit de la réaction est donc H2O
3)expérience 1: masse de CO2:0,22g
expérience 2 et 3: masse de CO2: 0,44g
ok pour moi 
Il te faut les quantités de matière. Ensuite tu fais ton tableau. Tu as déjà vu ça en classe ?
Non, je n'ai pas encore vu ça en classe, j'ai regardé ce que c'était sur internet mais je t'avoue que je ne suis pas sur d'avoir compris.
Merci en tout cas pour ton aide
non, vraiment, je ne m'en sors pas. Tant pis, je vais me coucher, je verrai demain.
Merci quand même
Re bonjour, après une bonne nuit de sommeil, j'ai essayé de comprendre le tableau d'avancement.
J'ai trouvé des choses mais je n'arrive pas à trouver la quantité de matière initiale de l'hydrogène pour pouvoir faire mes formules
n=m/M ou n=CxV.est ce que je dois prendre
m(H+)=m1-m(NaHCO3)= 90,84g- 0,84g=90g;cela me parait bizarre.
Merci de bien vouloir m'aider encore un peu, s'il vous plait
Oui,je connais les formules et j'ai réussi à trouver la quantité de matière du d'hydrogénocarbonate de sodium(1x10 puissance-2 mol)mais je n'arrive pas à trouver la quantité de matière pour l'hydrogène .Je connais seulement le volume mais je n'ai pas la concentration molaire et pour la masse, je pensais prendre m1 comme masse globale et faire m1-m(NaHCO3) avec 90,84-0,84g mais je ne sais pas si c'est ça.
Merci de me dire si c'est bon ou pas.
Alors, j'ai enfin fini mon tableau d'avancement mais j'aimerai si possible que quelqu'un vérifie mes calculs parce que comme je n'ai jamais fait de tableau, je ne suis pas sûr.
x/ avancement/ NaHCO3(s)+H+(aq)->CO2(g)+Na+(aq)+H2O(l)
Etat initial: 0/n(NaHCO3(s)=1x10-²/n(H+)=90mol/0/0/0
Etat intermédiaire:x/1x10-²-x/n(H+)-x=90-x /x/x/x
Etat final: xmax/1x10-²-xmax=1x10-²-1x10-²=0 /n(H+)-xmax=90-xmax=90-1x10-²= 89,99mol/1x10-²/1x10-²/1x10-²
Donc, je pense que l'hydrogène est en excès et
5) Le réactif dont dépend la quantité de produit formé est le NaHCO3(s)car c'est le réactif limitant.
Désolé, je ne sais pas faire un tableau sur le message le"/" correspond à la séparation de colonnes.
Merci de bien vouloir corrigé, stp
Bonjour, est ce que quelqu'un pourrait juste me dire si c'est juste ce que j'ai fait,svp.
Merci d'avance
Salut,
4)
m(H+)=m1-m(NaHCO3)= 90,84g- 0,84g=90g;cela me parait bizarre.
c'est effectivement faux
tu n'as pas besoin de calculer la quantité de H+ initial
l'expérience 3 et 2 montrent que à la 3 H+ est en excès car si on prend Vacide 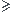 100 mL alors on a la même quantité de CO2 formée
100 mL alors on a la même quantité de CO2 formée
l'expérience 1 et 2 montrent que à la 1 NaCHO3 est en excès car si on prend Vacide 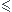 100 mL alors on n'a pas toujours la même quantité de CO2 formée alors qu'on met la même quantité de NaCHO3.
100 mL alors on n'a pas toujours la même quantité de CO2 formée alors qu'on met la même quantité de NaCHO3.
pour t on tableau d'avancement, merci d'utiliser la fonction tableau (l'icone quadrillée en haut à droite de l'aperçu)
| x | avancement | NaHCO3-+H+(aq)-->CO2(g)+Na+(aq)+H2O(l) | ||||
| Etat initial | 0 | n(NaHCO3)(s)=1x10-² | n(H+)=90mol | 0 | 0 | 0 |
| Etat intermédiaire | x | 1x10-²-x | n(H+)-x=90-x | x | x | x |
| Etat final | xmax | 1x10-²-xmax=1x10-²-1x10-²=0 | n(H+)-xmax=90-1x10-²=89,99mol | xmax=1x10-² | xmax=1x10-² | xmax=1x10-² |
Voilà ce que mon tableau donne mais si 90 est faux qu'est ce que je dois mettre dans le tableau pour n(H)+.
Merci de m'aider,svp
je viens de lire en entier ton énoncé, il n'est pas nécessaire de faire un tableau d'avancement
4. En comparant la composistion des réactifs et celle des produits , déterminer, pour chacun des systèmes, le réactif en excés(celui qui n'est pas totalement consommé).
expérience 1 : NaCHO3 en exces
expérience 3 : H+ en exces
on en déduit que pour la 2 soi H+ es en exces soit on a un mélange en proportion stoechiométrique
5. En déduire de quel réactif dépend la quantité de produit formé.
la quantité de produit formé dépend du réactif limitant qui est :
- ... pour l'expérience 1
- ... pour l'expérience 2
- ... pour l'expérience 3
Merci pour ton aide.
Dire que depuis hier je suis sur ce tableau d'avancement que je n'avais jamais fait en plus....
Pour la 5ème question, je pense que pour la 1 expérience le réactif limitant est le (H+), pour la 3, c'est le (NaHCO3) et pour la 2, je pense aussi que c'est (NaHCO3) mais je ne suis pas sur du tout.Qu'en penses tu?
il y a 2 réactifs, à la 4 on donne le réactif en exces le limitant c'est l'autre:
donc effectivement
expérience 1 : NaCHO3 en exces => H+ limitant
expérience 2 : H+ en exces => NaCHO3 limitant
expérience 3 : H+ en exces => NaCHO3 limitant


